
| A. | D2O与H2O是同位素 | B. | SiH4的稳定性>CH4的稳定性 | ||
| C. | 氢氟酸的酸性>盐酸的酸性 | D. | NaH是离子化合物 |
分析 A.同位素是质子数相同,中子数不同的同种元素的不同原子,D2O与H2O是分子;
B.非金属性越强,氢化物稳定性越强;
C.氢氟酸为弱酸,盐酸为强酸;
D.NaH由钠离子和H-离子组成,属于离子化合物.
解答 解:A.同位素的研究对象为原子,D2O与H2O是分子,所以二者不属于同位素,故A错误;
B.同主族从上到下非金属性依次减弱,则非金属性C>Si,非金属性越强氢化物越稳定,所以SiH4的稳定性<CH4的稳定性,故B错误;
C.氢氟酸为弱酸,盐酸为强酸,所以氢氟酸的酸性<盐酸的酸性,故C错误;
D.NaH由阳离子钠离子和阴离子H-离子组成,其电子式为Na+[:H]-,属于离子化合物,故D正确;
故选D.
点评 本题考查较为综合,涉及同位素、氢化物稳定性、酸性强弱比较及离子化合物等知识,题目难度不大,明确元素周期律内容为解答关键,注意掌握同位素、离子化合物的概念及判断方法,试题侧重基础知识的考查,有利于提高学生的灵活应用能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:实验题
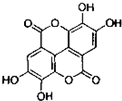 ).
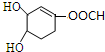
).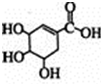 +Br2→
+Br2→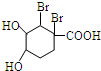 .
.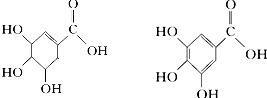
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲酸能与水以任意比互溶 | |
| B. | 1 mol•L-1甲酸溶液的pH约为2 | |
| C. | 10 mL 1 mol•L-1甲酸恰好与10 mL 1 mol•L-1NaOH溶液完全反应 | |
| D. | 甲酸溶液的导电性比盐酸溶液的弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3(CH2)15SO3Na | B. | 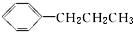 | C. | CCl4 | D. | CH3(CH2)4COOCH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑤ | B. | ①②④⑤ | C. | ③⑤ | D. | ④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酒精灯的使用,酒精灯熄灭时不能用嘴吹灭 | |
| B. | 温度计的使用,温度计不仅可以测量温度,还可以用于物质溶解时的搅拌 | |
| C. | 托盘天平的使用,潮湿的或具有腐蚀性的药品,必须放在玻璃器皿里称量,其他固体药品可直接放在天平托盘上称量 | |
| D. | 试管的加热,手持试管给固体或液体加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 酶是具有催化作用的蛋白质 | |
| B. | 酶的催化作用具有选择性和专一性 | |
| C. | 高温或重金属盐能使酶失去生理活性 | |
| D. | 酶只有在强酸性或强碱性条件下才能发挥作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温时,A能稀盐酸反应生成氢气,而B不能 | |
| B. | A原子的最外层电子数比B原子的最外层电子数少 | |
| C. | A原子电子层数比B原子电子层数多 | |
| D. | 等物质的量的A、B分别与足量的酸反应生成的氢气A比B多 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com