
| 阳极 | 阴极 | 溶液甲 | 物质乙 | |
| A | Pt | Pt | CuCl2 | CuCl2固体 |
| B | Pt | Pt | H2SO4 | H2O |
| C | Pt | Pt | NaCl | 盐酸 |
| D | Pt | Pt | CuSO4 | CuO |
| A. | A | B. | B | C. | C | D. | D |
分析 电解质在通电一段时间后要想让电解质复原要加入遵循:出什么加什么的原则,根据电解池的工作原理来回答.
解答 解:A、以铂为电极,电解氯化铜的水溶液实质是电解物质本身,要想复原,需要加CuCl2固体,故A正确;
B、以铂为电极,电解H2SO4溶液,实质是电解水,要想复原,需要加水,故B正确;
C、以Pt为阳极,电解氯化钠溶液会在两极上析出氢气和氯气,要想复原,则需通入氯化氢气体,加盐酸会多加入水,故C错误;
D、以Pt为阳极,电解硫酸铜,两极上分别产生金属铜和氧气,要想复原,则需加入CuO,故D正确;
故选:C.
点评 本题主要考查学生电解原理的应用知识以及电解质复原需加入的物质的选择,可以根据所学知识进行回答,难度不大.


科目:高中化学 来源: 题型:解答题
| 实验操作 | 预期现象与结论 |
| 步骤1:将适量稀H2SO4加入少许样品于试管中,加热溶解; | 溶液呈黄绿色,说明溶液中可能含Fe2+和Fe3+. |
| 步骤2:取少量溶液,滴 加0.01mol/L的KMnO4溶液. | 若紫红色不褪去,则说明催化剂中含铁元素的价态+3价;若紫红色褪去, 则说明催化剂中含有铁元素的价态为+2价 |
| 步骤3:另取少量溶液,滴 加20%的KSCN溶液. | 若溶液变为血红色,则说明催化剂中含铁元素的价态+3价;若溶液无变化,则说明催化剂中含铁元素的价态+2价; |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | MgCl2 的物质的量浓度为0.5mol•L-1 | |
| B. | Cl-的个数为3.01×1023 | |
| C. | Mg2+的物质的量为2mol | |
| D. | Cl-的物质的量浓度为2mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯和苯都能与溴水反应 | |
| B. | 甲烷、乙烯和苯在工业上都可通过石油分馏得到 | |
| C. | 有机物分子中都存在碳碳单键 | |
| D. | 乙醇可以被氧化为乙酸,二者都能发生酯化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2+3Mg$\frac{\underline{\;点燃\;}}{\;}$Mg3N2 | B. | N2+3H2$?_{催化剂}^{高温、高压}$2NH3 | ||
| C. | 2NO+O2═2NO2 | D. | N2+O2$\frac{\underline{\;放电\;}}{\;}$2NO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 中子数为18的硫离子:${\;}_{16}^{32}$S2- | |
| B. | S2-的结构示意图: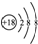 | |
| C. | Na2O2的电子式:Na+[${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$]2-Na+ | |
| D. | 亚硫酸的电离方程式:H2SO3?2H++SO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 步骤 | 实验操作 | 实验现象及数据 |
| ① | 取wgM粉末溶于过量的盐酸 | 产生气体X在标准状况下的体积为224mL,并得到无色溶液 |
| ② | 向步骤①所得的溶液中滴加氨水,调节pH至6,过滤、洗涤、灼烧、称重 | 固体Y的质量为1.020g |
| ③ | 向步骤②所得的滤液中滴加氢氧化钠溶液,调节pH至12,过滤、洗涤、灼烧、称重 | 固体Z的质量为1.200g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com