

分析 (1)氯气为有毒的气体;
(2)漂白粉的主要成分为Ca(ClO)2、CaCl2,有效成分是Ca(ClO)2,漂白液的有效成分为NaClO;
(3)氢气与氯气反应生成HCl,溶于水得到盐酸;氯水中HClO不稳定,若变质生成盐酸,酸性增强;
(4)MnO2完全反应,根据n=$\frac{m}{M}$计算8.7g的MnO2的物质的量,再根据方程式计算氯气的体积,被氧化的HCl生成生成氯气,根据氯原子守恒可知n被氧化(HCl)=2n(Cl2),根据m=nM计算质量.
解答 解:(1)氯气为有毒的气体,则①中钢瓶上应贴的标签为C,不易燃、易爆,本身不具有腐蚀性,故答案为:C;
(2)A.漂白粉的主要成分为Ca(ClO)2、CaCl2,漂白液的有效成分为NaClO,均为混合物,故A错误;
B.漂白粉的有效成分是Ca(ClO)2,含ClO-具有强氧化性,可用于漂白,故B正确;
C.石灰水的浓度较小,工业上将氯气通入石灰乳中制取漂白粉,故C错误;
D.过氧化钠与水反应,而漂白液的有效成分是NaClO,故D错误;
故答案为:B;
(3)氢气与氯气反应生成HCl,溶于水得到盐酸,发生的反应为H2+Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl;氯水中HClO不稳定,若变质生成盐酸,酸性增强,可选紫色石蕊检验,氯水、盐酸与A、B、C混合的现象均相同,不能鉴别,故答案为:H2+Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl;D;
(4)8.7g的MnO2的物质的量=$\frac{8.7g}{87g/mol}$=0.1mol,则:
MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O
1mol 22.4L
0.1mol V
V=$\frac{0.1mol×22.4L/mol}{1mol}$=2.24L;
被氧化的HCl生成氯气,根据氯原子守恒可知n被氧化(HCl)=2n(Cl2)=2×$\frac{2.24L}{22.4L/mol}$=0.2mol,
m被氧化(HCl)=0.2mol×36.5g/mol=7.3g;
故答案为:2.24;7.3g.
点评 本题考查较综合,涉及物质的性质、氧化还原反应计算等,注重高频考点的考查,把握氯气的性质、氯水的成分及物质性质与用途的关系等为解答的关键,侧重分析、应用及计算能力的考查,题目难度不大.


 智能训练练测考系列答案
智能训练练测考系列答案科目:高中化学 来源: 题型:选择题
| A. | 反应中转移3个电子 | B. | Fe2O3发生还原反应 | ||
| C. | CO被还原 | D. | CO为氧化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 79、81 | B. | 45、46 | C. | 44、45 | D. | 44、46 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X元素最高价氧化物对应的水化物一定是强酸 | |
| B. | X元素氢化物的化学式一定为H2X | |
| C. | X的单质一定是良好的半导体材料 | |
| D. | X元素的氧化物一定能与烧碱反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
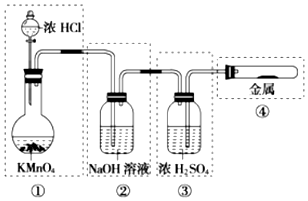
| A. | ①和②处 | B. | ②处 | C. | ②和③处 | D. | ②③④处 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 气体A为SO2和H2的混合物 | B. | 气体A中SO2和H2的体积比为4:1 | ||
| C. | 反应中共消耗Zn 97.5g | D. | 反应中共转移3mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X3Y2 | B. | X2Y | C. | Y3X2 | D. | Y2X3 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 在标准状态下,1L庚烷完全燃烧后,所生成的气态产物的分子数为$\frac{7}{22.4}$NA | |
| B. | 1mol碳正离子CH5+所含的电子数为10NA | |
| C. | 标准状态下,16g甲烷完全燃烧所消耗的氧气的分子数为2NA | |
| D. | 0.5mol C3H8分子中含C-H共价键2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com