������һ����Ҫ�Ļ���ԭ�ϣ���ҵ�������������Ҫ�������£�
��1����N
2��H
2Ϊԭ�Ϻϳɰ�������ӦN
2��g��+3H
2��g��?2NH
3��g����H��0
�����д�ʩ�������H
2��ת�����ǣ���ѡ����ţ�
��
a��ѡ���ʵ��Ĵ��� b������ѹǿ c����ʱ�������ɵ�NH
3 d�������¶�
��һ���¶��£����ܱ������г���1molN
2��3molH
2������Ӧ���������ݻ��㶨���ﵽƽ��״̬ʱ�������ڵ�ѹǿ��ԭ����
����N
2��ת����a
1=
��
������ѹǿ�㶨���ﵽƽ��״̬ʱ��N
2��ת����Ϊa
2����a
2
a
1�����������������=������
��2������������Ϊ��Ҫԭ�������ᣮ
��NH
3����������������NO�ķ�Ӧ�Ļ�ѧ����ʽ��
��
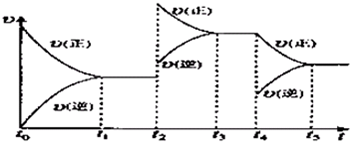
�����ݻ��㶨���ܱ������н��з�Ӧ2NO��g��+O
2��g��?2NO
2��g����H��0
�÷�Ӧ�ķ�Ӧ���ʣ�v����ʱ�䣨t���仯�Ĺ�ϵ��ͼ��ʾ����t
2��t
4ʱ��ֻ�ı�һ������������˵����ȷ���ǣ���ѡ����ţ�
��
a����t
1��t
2ʱ�������������������ѹǿ���ֲ����жϷ�Ӧ�Ѵﵽƽ��״̬
b����t
2ʱ����ȡ�Ĵ�ʩһ���������¶�
c����t
3��t
4ʱ��������������������ܶȱ��ֲ����жϷ�Ӧ�Ѵﵽƽ��״̬
d����t
0��t
5ʱ��������NO
2�����������t
3ʱֵ�����
�����ݻ���ͬ���¶ȷֱ�ΪT
1��T
2�������ܱ������зֱ�������NO
2������Ӧ��
2NO
2 ��g��?N
2O
4��g����H��0�����º����·�Ӧ��ͬʱ��ֱ�ⶨ��ϵ��NO
2�İٷֺ����ֱ�Ϊa
1��a
2����֪T1��T2����a
1
a
2 A������ B��С�� C������ D�����϶��п���
��3�����᳧��������2�ַ�������β����
�ٴ���ԭ������������ʱ��H
2��NO
2��ԭΪN
2��
��֪��2H
2��g��+O
2��g��=2H
2O��g����H=-483.5kJ/mol
N2��g��+2O
2��g��=2NO
2��g����H=+133kJ/mol
��H
2��ԭNO
2����ˮ������Ӧ���Ȼ�ѧ����ʽ��
��
�ڼ�Һ���շ�����Na
2CO
3��Һ����NO
2����CO
2��
��ÿ9.2gNO
2��Na
2CO
3��Һ��Ӧʱת�Ƶ�����Ϊ0.1mol����Ӧ�����ӷ���ʽ��
��



 �����ѧСѧ�꼶�νӽݾ��㽭��ѧ������ϵ�д�
�����ѧСѧ�꼶�νӽݾ��㽭��ѧ������ϵ�д�
 ��һ�������������Ժ�CO2������Ӧ��Fe��s��+CO2��g��
��һ�������������Ժ�CO2������Ӧ��Fe��s��+CO2��g�� FeO��s��+CO��g������H��0
FeO��s��+CO��g������H��0