
【题目】把一端弯成螺旋状的铜丝放在酒精灯火焰上加热,看到铜丝表面生成黑色的___(填化学式),再迅速把铜丝插入盛有乙醇的试管里,看到铜丝表面___,反复多次,试管内有___气味的___生成,其反应的化学方程式为___,反应中乙醇被___。
【答案】CuO 变红 刺激性 乙醛 2CH3CH2OH+O2![]() 2CH3CHO+2H2O 氧化
2CH3CHO+2H2O 氧化
【解析】
铜丝在空气中燃烧生成CuO,化学方程式为:![]() ,加热过的铜丝插入盛有乙醇的试管中,氧化铜与乙醇反应生成乙醛与铜,该变化中,铜丝起催化剂作用,乙醇在催化剂、加热条件下与氧气反应生成乙醛与水。
,加热过的铜丝插入盛有乙醇的试管中,氧化铜与乙醇反应生成乙醛与铜,该变化中,铜丝起催化剂作用,乙醇在催化剂、加热条件下与氧气反应生成乙醛与水。
铜丝在空气中燃烧,铜丝表面生成黑色的CuO;再迅速把铜丝插入盛有乙醇的试管里,氧化铜与乙醇反应生成乙醛与铜,看到铜丝表面变红,反应方程式为:2CH3CH2OH+O2![]() 2CH3CHO+2H2O,反复多次,试管内产生刺激性气味的乙醛气体,该反应铜做催化剂,乙醇被氧化;故答案为:CuO;变红;刺激性;乙醛;2CH3CH2OH+O2
2CH3CHO+2H2O,反复多次,试管内产生刺激性气味的乙醛气体,该反应铜做催化剂,乙醇被氧化;故答案为:CuO;变红;刺激性;乙醛;2CH3CH2OH+O2![]() 2CH3CHO+2H2O;氧化。
2CH3CHO+2H2O;氧化。


 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是( )
A.当一个可逆反应达到平衡状态时,就是这个反应在该条件下所能达到的限度
B.当一个可逆反应达到平衡状态时,这个反应的正反应速率和逆反应速率相等
C.可以通过控制反应条件,使2 mol SO2与1 mol O2反应生成2 mol SO3
D.化学反应的限度可以通过改变条件来改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,某些花岗岩会产生氡(![]() Rn),从而对人体产生伤害。请回答:
Rn),从而对人体产生伤害。请回答:
(1)该原子的质量数是________,质子数是________,中子数是________。
(2)研究发现,镭能蜕变为![]() Rn,故将
Rn,故将![]() Rn称为镭射气;钍能蜕变为
Rn称为镭射气;钍能蜕变为![]() Rn,故将
Rn,故将![]() Rn称为钍射气;锕能蜕变为
Rn称为钍射气;锕能蜕变为![]() Rn,故将
Rn,故将![]() Rn称为锕射气。
Rn称为锕射气。![]() Rn、
Rn、![]() Rn、
Rn、![]() Rn________。
Rn________。
A.属于同种元素 B.互为同位素
C.属于同种核素 D.属于同种原子
(3)由(2)可知,________决定元素种类,________决定核素种类。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知100℃时,水的离子积常数Kw=1×10-12,对于该温度下pH=l1的氨水,下列叙述正确的是
A. 向该溶液中加入同温同体积pH=1的盐酸,反应后溶液呈中性
B. 温度降低至25℃,该氨水溶液中H2O电离出的H+浓度小于10-11mol/L
C. 该氨水溶液中加入NH4Cl溶液,NH3·H2O的电离能力增强
D. 滴加等浓度等体积的硫酸,得到的溶液中存在电离平衡:NH4HSO4(aq)![]() NH4+(aq)+H+(aq)+SO42-(aq)
NH4+(aq)+H+(aq)+SO42-(aq)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】举世瞩目的中国探月工程三期再入返回试验器于2014年10月24日凌晨成功发射,为实现月球采样和首次地月往返踏出了成功的第一步。探月工程三期的主要目标是实现无人自动采样返回,突破月面采样、月面上升、月球轨道交会对接等核心关键技术。已知所用火箭推进剂为肼 (N2H4)和过氧化氢(H2O2),火箭箭体一般采用钛合金材料。
请回答下列问题:
(1)N2H4、H2O2分子中电负性最大的元素在周期表中的位置为_______,第一电离能最大的元素为_______。
(2)钛的原子序数为22,其基态电子排布式示意图为________________。
(3)1 mol N2H4分子中含有的键数目为_______。
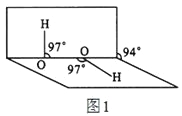
(4)H2O2分子结构如图1,其中心原子杂化轨道为_______,估计它难溶于CS2,简要说明原因___________。
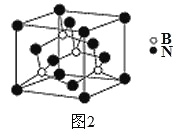
(5)氮化硼其晶胞如图2所示,则处于晶胞顶点上的原子的配位数为___,若立方氮化硼的密度为ρ g·cm-3,阿伏加德罗常数为NA,则两个最近N原子间的距离为________cm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语表达不正确的是
A.用稀硝酸洗涤做过银镜反应的试管:Ag+4H++NO3- =Ag++NO↑+2H2O
B.HClO的结构式:H-O-Cl
C.Na2CO3溶液呈碱性的原因:CO32-+ H2O![]() HCO3-+ OH-
HCO3-+ OH-
D.CH4的球棍模型:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着环境污染的加重和人们环保意识的加强,生物降解材料逐渐受到了人们的关注。以下是PBA(一种生物降解聚酯高分子材料)的合成路线:

已知:①烃A的相对分子质量为84,核磁共振氢谱显示只有1组峰,不能使溴的四氯化碳溶液褪色。
②化合物C中只含一个官能团。
③R1CH=CHR2 ![]() R1COOH+R2COOH。
R1COOH+R2COOH。
④RC≡CH+ →
→ 。
。
请回答下列问题:
(1)由A生成B的反应类型为______________。
(2)由B生成C的化学方程式为____________________________。
(3)E的结构简式为____________________________________。
(4)F的名称为__________(用系统命名法);由D和F生成PBA的化学方程式为____________________________;
(5)E的同分异构体中能同时满足下列条件的共有_________种。(不含立体异构)
①链状化合物②能发生银镜反应③氧原子不与碳碳双键直接相连
其中,核磁共振氢谱显示为2组峰,且峰面积比为2∶1的是_________(写结构简式)。
(6)若由1,3丁二烯为原料(其他无机试剂任选)通过三步制备化合物F,其合成路线为__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式的书写及评价,均合理的是
选项 | 离子方程式 | 评价 |
A | 用铜电极电解饱和KCl溶液:2H2O+2Cl- | 正确:Cl-的失电子能力比OH-强 |
B | 向CuSO4溶液中通入过量的H2S气体:Cu2++H2S=CuS↓+2H+ | 错误:H2S的酸性比H2SO4弱 |
C | Ba(HCO3)2溶液与足量的NaOH溶液反应:Ba2++HCO3- +OH- ═BaCO3↓+H2O | 错误:Ba2+与HCO3-系数比应为1:2 |
D | 过量SO2通入到NaClO溶液中:SO2+ClO- +H2O= HClO+HSO3- | 正确:H2SO3的酸性比HClO强 |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com