
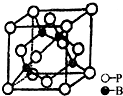
 磷是生物体中不可缺少的元素之一,它能形成多种化合物.
磷是生物体中不可缺少的元素之一,它能形成多种化合物.分析 (1)P原子核外有15个电子,分三层排布,即有三个能层,最外层M能层为3s2p3,s能级有1个轨道,p能级有3个轨道,据此分析判断;
(2)同一周期元素自左而右第一电离能呈增大趋势,但P元素原子3p能级是半满稳定状态,能量较低,第一电离能高于同周期相邻元素;
(3)P4分子为正四面体构型,键角为60°,P4分子中每个P原子与相邻的3个P原子形成3个σ键、并且含有1对孤对电子,杂化轨道数目为4;依据相似相溶的原理进行解答;
(4)Fe原子核外电子数为26,原子形成阳离子先按能层高低失去电子,能层越高的电子越容易失去,同一能层中按能级高低失去电子,能级越高越容易失去;同周期元素从左到右元素的电负性逐渐增强,则电负性:S>P,同主族元素从上到下电负性逐渐减弱,则电负性:O>S,由此分析解答;
(5)该晶胞中P原子个数=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,B原子个数为4,再根据ρ=$\frac{m}{V}$计算密度.
解答 解:(1)P原子核外有15个电子,分三层排布,即有三个能层,所以电子占据的最高能层符号为M;最外层为3s2p3,则磷元素位于周期表的p区,s能级有1个轨道,p能级有3个轨道,所以M能层具有的原子轨道数为4个;故答案为:p;M;4;
(2)同一周期元素自左而右第一电离能呈增大趋势,但P元素原子3p能级是半满稳定状态,能量较低,第一电离能高于同周期相邻元素,故铝到磷元素的第一电离能P>S>Si>Al,所以第三周期中第一电离能位于铝元素和磷元素之间的有2种,故答案为:2;
(3)P4分子为正四面体构型,键角为60°,P4分子中每个P原子与相邻的3个P原子形成3个σ键、含有1对孤对电子,杂化轨道数目为4,则P原子采取sp3杂化;
因为P4分子中每个P原子与相邻的3个P原子形成3个σ键,则平均每个P原子形成1.5个σ键,所以3.1g白磷中σ键的数目为$\frac{3.1g}{31g/mol}$×1.5=0.15mol;
相似相溶原理是指由于极性分子间的电性作用,使得极性分子组成的溶质易溶于极性分子组成的溶剂,难溶于非极性分子组成的溶剂;非极性分子组成的溶质易溶于非极性分子组成的溶剂,难溶于极性分子组成的溶剂,P4和CO2是非极性分子,H2O是极性分子,根据相似相溶的原理,P4易溶于CO2,难溶于水,
故答案为:60°;sp3;0.15mol;P4和CO2是非极性分子,H2O是极性分子,根据相似相溶的原理,P4易溶于CO2,难溶于水;
(4)Fe原子核外有26个电子,核外电子排布为1s22s22p63s23p63d64s2,Fe原子失去4s能级2个电子、3d能级1个电子形成Fe3+,Fe3+电子排布式为1s22s22p63s23p63d5;同周期元素从左到右元素的电负性逐渐增强,则电负性:S>P,同主族元素从上到下电负性逐渐减弱,则电负性:O>S,所以电负性O>P,又Fe为金属元素,则电负性由大到小的顺序是O>P>Fe,故答案为:1s22s22p63s23p63d5;O>P>Fe;
(5)该晶胞中P原子个数=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,B原子个数为4,晶胞边长=a×10-10cm,体积V=(a×10-10cm)3,ρ=$\frac{m}{V}$=$\frac{\frac{4}{N{\;}_{A}}×42}{(a×10{\;}^{-10}){\;}^{3}}$g•cm3=$\frac{168}{(a×10{\;}^{-10}){\;}^{3}N{\;}_{A}}$g•cm3,
故答案为:$\frac{168}{(a×10{\;}^{-10}){\;}^{3}N{\;}_{A}}$g•cm3.
点评 本题考查物质结构和性质,涉及电负性的比较、杂化方式的判断、晶胞的计算、电子排布式等,侧重于基础知识的综合应用的考查,题目难度较大,注意把握晶胞的计算方法.


科目:高中化学 来源: 题型:选择题
| A. | 乙酸和乙酸乙酯可用Na2CO3溶液加以区别. | |
| B. | 戊烷(C5H12)有两种同分异构体 | |
| C. | 乙烯、聚乙烯分子中均含有碳碳双键 | |
| D. | 二氯甲烷有两种同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 胶体不稳定,静置后容易产生沉淀 | |
| B. | 可用丁达尔效应区别溶液与悬浊液 | |
| C. | 溶液中溶质粒子不能通过半透膜,胶体中分散质粒子能透过半透膜 | |
| D. | 胶体与其他分散系的本质区别是分散质粒子直径在1 nm~100nm之间 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
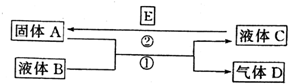 中学化学中有很多物质可以实现图中物质之间的转化.其中反应条件和部分反应的产物已略去.液体B和C可能是单一溶质的溶液,也可能是纯净物.
中学化学中有很多物质可以实现图中物质之间的转化.其中反应条件和部分反应的产物已略去.液体B和C可能是单一溶质的溶液,也可能是纯净物.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用品: 有效成分:NaCl用途:做调味品 有效成分:NaCl用途:做调味品 | |
| B. | 用品: 有效成分:Na2CO3用途:做发酵粉 有效成分:Na2CO3用途:做发酵粉 | |
| C. | 用品: 有效成分:Al(OH)3用途:做抗酸药 有效成分:Al(OH)3用途:做抗酸药 | |
| D. | 用品: 有效成分:Ca(ClO)2用途:做消毒剂 有效成分:Ca(ClO)2用途:做消毒剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
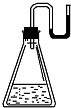 有下列物质:①NaOH固体;②浓硫酸;③NH4NO3晶体;④金属钠.现将它们分别装入有水的锥形瓶里,立即塞紧带U形管的塞子,发现U形管内的滴有红墨水的水面呈形如图所示状态,判断加入的物质可能是( )
有下列物质:①NaOH固体;②浓硫酸;③NH4NO3晶体;④金属钠.现将它们分别装入有水的锥形瓶里,立即塞紧带U形管的塞子,发现U形管内的滴有红墨水的水面呈形如图所示状态,判断加入的物质可能是( )| A. | ①②③④ | B. | ①②④ | C. | ②③④ | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 55 kJ | B. | 220 kJ | C. | 1108 kJ | D. | 550 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷和Cl2的反应与乙烯和Br2的反应属于同一类型的反应 | |
| B. | 分子式为C4H7ClO2,可与NaHCO3产生CO2的有机物可能结构有3种 | |
| C. | 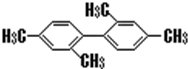 分子中至少有11个碳原子处于同一平面上 分子中至少有11个碳原子处于同一平面上 | |
| D. | 1mol有机物 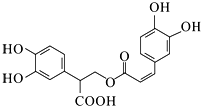 一定条件下能和7molNaOH反应 一定条件下能和7molNaOH反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向银氨溶液中加入足量氢溴酸溶液:Ag(NH3)2++OHˉ+3H+═Ag++2NH4++H2O | |
| B. | 向0.1 mol/L pH=1的NaHA的溶液中加入NaOH溶液:HA-+OH-═H2O+A2- | |
| C. | H2C2O4使酸性KMnO4溶液褪色:2MnO4-+5H2C2O4+6H+═2Mn2++10CO2↑+8H2O | |
| D. | NH4Al(SO4)2溶液中加入Ba(OH)2溶液使SO42-完全沉淀:2Ba2++2SO42-+4OH-+Al3+═2BaSO4↓+AlO2-+2H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com