
| A. | c=$\frac{w•1000•ρ}{M}$ | B. | m=$\frac{Vρw}{100}$ | C. | c=$\frac{1000m}{(V•M)}$ | D. | w=$\frac{cM}{1000ρ}$ |
分析 溶液的质量为ρV,溶质的质量等于溶液的质量与质量分数的乘积,再结合c=$\frac{n}{V}$、W=$\frac{m(溶质的质量)}{m(溶液的质量)}$×100%对各选项进行判断.
解答 解:A.c=$\frac{n}{V}$=$\frac{\frac{m}{M}}{V}$=$\frac{\frac{Vρ×W}{M}mol}{V×1{0}^{-3}L}$=$\frac{1000wρ}{M}$,故A正确;
B.m=m(溶液)×W=ρVW,故B错误;
C.c=$\frac{n}{V}$=$\frac{1000m}{VM}$mol/L,故C正确;
D.W=$\frac{m(溶质的质量)}{m(溶液的质量)}$×100%=$\frac{V×1{0}^{-3}L×cmol/L×Mg/mol}{Vρ}$×100%=$\frac{cM}{1000ρ}$×100%,则W%=$\frac{cM}{1000ρ}$%,故D正确;
故选B.
点评 本题考查物质的量与其浓度的综合应用,题目难度中等,试题侧重于物质的量的相关计算公式的综合运用,注意把握相关计算公式,试题培养了学生的化学计算能力.


 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:选择题
| A. | 1个 | B. | 2 | C. | 3 | D. | 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
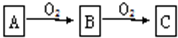
 2SO3.
2SO3.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol/L | B. | 0.2mol/L | C. | 0.3mol/L | D. | 0.4mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
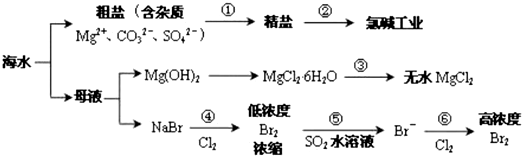
| A. | 过程①除杂的顺序:NaOH 溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸 | |
| B. | 在过程③中将MgCl2•6H2O 灼烧即可制得无水 MgCl2 | |
| C. | 在过程④、⑥反应中每氧化 0.2 mol Br- 需消耗2.24 LCl2 | |
| D. | 从第④步到第⑥步的目的是为了富集溴 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| A | B | ||||||
| D | E | F | |||||
| C | G | H |
 ;
; +HNO3$→_{50~60℃}^{浓硫酸}$
+HNO3$→_{50~60℃}^{浓硫酸}$ +H2O,反应类型取代反应.
+H2O,反应类型取代反应.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | ① | ② | ③ | 实验结论 |  |
| A | 稀硝酸 | Na2S | AgNO3与 AgCl的浊液 | Ksp(AgCl)>Ksp(Ag2S) | |
| B | 浓硫酸 | 无水 乙醇 | 溴水 | 有乙烯生成 | |
| C | 稀盐酸 | Na2SO3 | Ba(NO3)2 溶液 | SO2与可溶性钡盐均可以生成白色沉淀 | |
| D | 稀硫酸 | Na2CO3 | Na2SiO3 溶液 | 酸性: 稀硫酸>碳酸>硅酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com