
| A、Na、Mg、Al还原性依次增强 |
| B、HCl、PH3、H2S稳定性依次减弱 |
| C、NaOH、KOH、CsOH碱性依次增强 |
| D、S2-、Cl-、K+、Ca2+离子半径依次增大 |


 优生乐园系列答案
优生乐园系列答案 新编小学单元自测题系列答案
新编小学单元自测题系列答案科目:高中化学 来源: 题型:
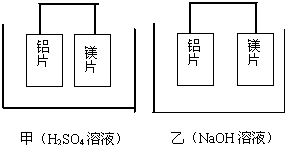 有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均使用镁片和铝片作电极,但甲同学将电极放入6mol/LH2SO4溶液中,乙同学将电极放入6mol/LNaOH溶液中,如图:
有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均使用镁片和铝片作电极,但甲同学将电极放入6mol/LH2SO4溶液中,乙同学将电极放入6mol/LNaOH溶液中,如图:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaClO溶液的消毒原理是使蛋白质变性 |
| B、1molCl2与足量NaOH溶液反应转移2mol电子 |
| C、NaClO溶液的漂白原理与Na2O2、SO2相同 |
| D、“84”消毒液与“洁厕灵”(盐酸)共同使用,可达到既清洁又消毒的双重效果 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、都是有机高分子化合物 |
| B、都可以看作为乙炔的加聚产物 |
| C、都能燃烧且一定条件下都可以与H2发生加成反应 |
| D、都有很高的熔点和硬度且难溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H-+OH+═H2O |
| B、H++OH+═H2O |
| C、H-+OH-═H2O |
| D、H++OH-═H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该溶液中含6.02×1022个HCl分子 |
| B、标准状况下2.24L HCl溶于1L水中所得的溶液 |
| C、将500mL 0.2mol/L的盐酸加水稀释到1L所得的溶液 |
| D、将2.0L 0.05mol/L的盐酸蒸发浓缩到体积为1L所得的溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向FeSO4溶液中通入过量Cl2 |
| B、向NaHCO3溶液中加入一定质量的Na2O2粉末 |
| C、向NaI和NaBr混合溶液中通入过量Cl2 |
| D、向NaOH溶液中加入过量AlCl3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com