
| A. | CO的燃烧热为566.0 kJ•mol-1 | |
| B. | 反应②△H<0,所以该反应能自发进行 | |
| C. | 使用催化剂能提高其转化率 | |
| D. | 根据①和②推知总反应为2CO(g)+SO2(g)=S(s)+2CO2 (g)△H=-270kJ•mol-1 |
分析 A.燃烧热为1mol可燃物完全燃烧放出的热量;
B.△H-T△S<0的反应可自发进行;
C.催化剂不影响平衡移动;
D.由盖斯定律可知,①×2-②得到2CO(g)+SO2(g)=S(s)+2CO2 (g).
解答 解:A.燃烧热为1mol可燃物完全燃烧放出的热量,则CO的燃烧热为△H=-283.0 kJ•mol-1,故A错误;
B.△H-T△S<0的反应可自发进行,可知放热的反应不一定是自发的,故B错误;
C.催化剂不影响平衡移动,则转化率不变,故C错误;
D.由盖斯定律可知,①×2-②得到2CO(g)+SO2(g)=S(s)+2CO2 (g),△H=(-283.0kJ•mol-1)×2+296.0kJ•mol-1=-270kJ•mol-1,故D正确;
故选D.
点评 本题考查反应热与焓变,为高频考点,把握反应进行方向的判断、燃烧热、平衡移动等为解答的关键,侧重分析与应用能力的考查,注意选项D结合盖斯定律分析,题目难度不大.


科目:高中化学 来源: 题型:实验题
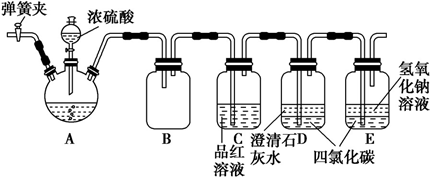
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 | |
| B. | 由H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ•mol-1可知,若将含5mol H2SO4的浓硫酸与含1mol NaOH的稀溶液混合,放出的热量大于57.3kJ | |
| C. | 由C(石墨)=C(金刚石)△H=+1.90kJ•mol-1可知,金刚石比石墨稳定 | |
| D. | 在101kPa时,2g H2完全燃烧生成液态水,放出285.8kJ热量,则氢气燃烧的热化学方程式为 2H2(g)+O2(g)=2H2O(l)△H=-285.8kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H5OH(l)+3O2(g)═2CO2(g)+3H2O(g)△H=-1367.0 kJ•mol-1(燃烧热) | |
| B. | NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=+57.3 kJ•mol-1(中和热) | |
| C. | S(s)+O2(g)═SO2(g)△H=-269.8 kJ•mol-1(反应热) | |
| D. | 2H2(g)+O2(g)═2H2O(l)△H=571.6kJ•mol-1(反应热) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 436 kJ | B. | 557 kJ | C. | 920 kJ | D. | 618 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室用CaCO3固体与稀盐酸制取CO2,多倒出的CaCO3固体不能再放回原试剂瓶 | |
| B. | H2还原灼热的氧化铜时,点燃酒精灯前必须先检验H2的纯度 | |
| C. | 含硫酸铜的废液倒入水槽,用水冲入下水道 | |
| D. | 少量浓硫酸沾在皮肤上,立即用氢氧化钠溶液冲洗 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验顺序 | 实验内容 | 实验现象 |
| ① | A+B | 没有明显变化 |
| ② | B+D | 有无色、无味气体生成 |
| ③ | B+C | 有白色沉淀生成 |
| ④ | A+D | 有白色沉淀生成 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com