
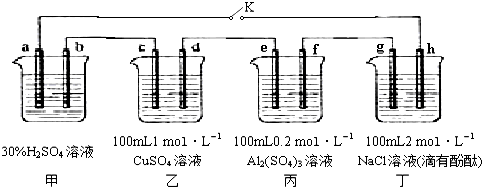
分析 甲池是原电池做电源,发生的反应为:Pb+PbO2+2H2SO4$?_{充电}^{放电}$2PbSO4+2H2O;乙丙丁是电解池,闭合K,发现G电极附近的溶液变红,说明G电极是电解池的阴极,H是电解池的阳极;所以a为正极,b为负极;c电极为阴极,d为阳极;e电极为阴极,f为阳极;20min后,将K断开,此时c、d两极上产生的气体体积相同,
(1)依据分析判断电极名称;
(2)丙中电解水;
(3)时c、d两极上产生的气体体积相同,c电极上发生的电极反应为:Cu2++2e-=Cu;2H++2e-=H2↑,d电极上发生的电极反应为:4OH--4e-=2H2O+O2↑,根据电子守恒计算生成的Cu、氢气和氧气的物质的量;
(4)20min后将乙装置与其他装置断开,然后在c、d两极间连上灵敏电流计,发现电流计指针偏转,说明形成了原电池反应,氢气在c极失电子,氧气在d极得电子;
(5)电解后丁装置中的溶液为氢氧化钠,根据转移电子守恒计算生成NaOH的浓度,加醋酸生成醋酸钠溶液,结合Ka=$\frac{c(C{H}_{3}CO{O}^{-})×c({H}^{+})}{c(C{H}_{3}COOH)}$计算.
解答 解:甲池是原电池做电源,发生的反应为:Pb+PbO2+2H2SO4$?_{充电}^{放电}$2PbSO4+2H2O;乙丙丁是电解池,闭合K,发现G电极附近的溶液变红,说明G电极是电解池的阴极,H是电解池的阳极;所以a为正极,b为负极;c电极为阴极,d为阳极;e电极为阴极,f为阳极;20min后,将K断开,此时c、d两极上产生的气体体积相同,
(1)a电极是铅蓄电池的正极,正极的电极材料是PbO2;
故答案为:PbO2;
(2)丙中电解硫酸铝,其实际上是电解水,其电解方程式为:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;
故答案为:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;
(3)时c、d两极上产生的气体体积相同,c电极上发生的电极反应为:Cu2++2e-=Cu;2H++2e-=H2↑,d电极上发生的电极反应为:4OH--4e-=2H2O+O2↑,
设生成的氧气为xmol,则氢气也为xmol,生成的Cu为0.1L×1mol/L=0.1mol,由得失电子可得:2x+0.1×2=4x,解得x=0.1mol,
则电解时生成0.1mol氢气、0.1mol氧气和0.1molCu,若要恢复到原来的状态,需要加入0.1molCu(OH)2;
故答案为:0.1molCu(OH)2;
(4)20min后将乙装置与其他装置断开,然后在c、d两极间连上灵敏电流计,发现电流计指针偏转,说明形成了原电池反应,氢气在c极失电子,c为负极,氧气在d极得电子,正极的反应为:O2+4H++4e-=2H2O;
故答案为:负;O2+4H++4e-=2H2O;
(5)电解后丁装置中的溶液为氢氧化钠,乙中电解生成0.1mol氧气,转移电子为0.4mol,则氯化钠被全部电解,则生成的氢氧化钠为0.2mol,其浓度2mol/L,加醋酸后溶液的pH恰好等于7,则c(H+)=c(OH-),由电荷守恒可知c(Na+)=c(CH3COO-)=$\frac{2mol/L×a×1{0}^{-3}L}{(a+b)×1{0}^{-3}L}$=$\frac{2a}{a+b}$mol/L,
c(CH3COOH)=$\frac{2mol/L×a×1{0}^{-3}L}{(a+b)×1{0}^{-3}L}$-c(CH3COO-)=$\frac{2(b-a)}{a+b}$mol/L,Ka=$\frac{c(C{H}_{3}CO{O}^{-})×c({H}^{+})}{c(C{H}_{3}COOH)}$=$\frac{\frac{2a}{a+b}×1{0}^{-7}}{\frac{2(b-a)}{a+b}}$=1.75×10-5,解得$\frac{a}{b}$=$\frac{175}{176}$;
故答案为:$\frac{175}{176}$.
点评 本题考查了原电池和电解池原理、电离常数在计算中的应用等,正确判断原电池正负极和电解池的阴阳极、以及电极方程式的书写方法是解本题关键,根据离子放电顺序确定阴阳极电极反应,并结合得失电子守恒解答,难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
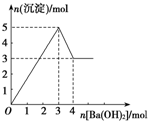 如图表示向某溶液中滴加Ba(OH)2溶液时,沉淀的物质的量随Ba(OH)2的物质的量的变化关系.该溶液的成分可能是( )
如图表示向某溶液中滴加Ba(OH)2溶液时,沉淀的物质的量随Ba(OH)2的物质的量的变化关系.该溶液的成分可能是( )| A. | MgSO4 | B. | KAl(SO4)2 | C. | Al2(SO4)3 | D. | Na AlO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 金属离子 | Fe3+ | Cu2+ |
| 氢氧化物开始沉淀时的pH | 1.9 | 4.7 |
| 氢氧化物完全沉淀时的pH | 3.2 | 6.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 如图甲、乙是电化学实验装置.请回答下列问题:
如图甲、乙是电化学实验装置.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4 LBr2所含溴原子的数目为2NA | |
| B. | 常温下,NO2与足量的水反应生成0.1molNO,转移的电子数为0.2NA | |
| C. | 1 mol 乙醇中含有的C-H键的数目为6NA | |
| D. | 1mol•L-1的NaClO溶液中含有的ClO-数目小于NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 粗铜与直流电源负极相连 | |
| B. | 相同时间内阳极质量变化与阴极质量变化可能不同 | |
| C. | 硫酸铜溶液浓度始终保持不变 | |
| D. | 杂质Ag以Ag2SO4的形式沉入电解槽形成“阳极泥” |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若溶液中c(Cl-)=c(NH4+),则溶液一定呈中性 | |
| B. | 若c(Cl-)>c(NH4+)>c(H+)>c(OH-),则溶质一定为NH4Cl | |
| C. | 若c(OH-)>c(H+),则溶液中不可能存在:c(NH4+)>c(OH-)>c(Cl-)>c(H+) | |
| D. | 若溶质为NH4Cl、NH3•H2O,则一定存在:c(NH4+)>c(OH-)>c(Cl-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作(或设计) | 实验现象 | 结论 |
| A | 向溶液中滴加经盐酸酸化的BaCl2溶液 | 溶液中产生白色沉淀 | 溶液中含有SO42- |
| B | 以镁、铝、氢氧化钠溶液构成原电池 | 镁表面有气泡产生 | 镁作原电池的负极 |
| C | 加热盛有NH4Cl固体的试管 | 试管底部固体消失,试管口有晶体凝结 | NH4Cl固体可以升化 |
| D | 向KI溶液中滴入少量溴水和苯,振荡、静置 | 上层溶液呈紫红色 | I-的还原性强于Br- |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com