
| A.10(a+b-12) % | B.10(a+b-14) % | C.10(12-a-b) % | D.10(14-a-b) % |
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案科目:高中化学 来源:不详 题型:单选题
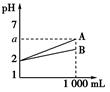
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 H++A-,回答下列问题:
H++A-,回答下列问题:查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NH3·H2O 的导电性比NaOH溶液弱得多 |
| B.0.1mol/L 的NH3·H2O 的pH值大于7 |
| C.NH4Cl 的水溶液的pH值小于7 |
| D.5mL 1mol/L的NH3·H2O跟10mL 0.5mol/L的HCl恰好完全反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1mol/L氢氰酸溶液的pH约为3 |
| B.HCN易溶于水 |
| C.10 mL1mol/LHCN恰好与10 mL 1mol/L NaOH溶液完全反应 |
| D.在相同条件下,HCN溶液的导电性比强酸溶液的弱 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.1 mol/L氨水与0.1 mol/L盐酸等体积混合,所得溶液中c(H+)=c(OH-) |
| B.100 ℃时,纯水中c(H +)=1×10-6 mol·L-1,此时纯水显酸性 |
| C.25℃时,将pH=a的醋酸溶液稀释10倍后,溶液的pH=b,则a>b |
D.25℃时, =0.1 mol/L的溶液中,Na+、CO32-、Cl-一定能大量共存 =0.1 mol/L的溶液中,Na+、CO32-、Cl-一定能大量共存 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com