
| A. | 硝酸铵和水 | B. | 浓硫酸和水 | C. | 生石灰和水 | D. | 苛性钠和水 |
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案科目:高中化学 来源: 题型:解答题


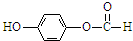 和
和 、
、 (其中两种)
(其中两种)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醛与新制Cu(OH)2悬浊液反应生成红色的Cu2O沉淀 | |
| B. | 银镜反应中醛发生的是还原反应 | |
| C. | 甲醛、乙醛、丙醛都没有同分异构体 | |
| D. | 醛类催化加氢后都能得到饱和一元醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
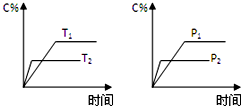 可逆反应aA(g)+bB(g)?cC(g)+dD(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图,下列叙述正确的是( )
可逆反应aA(g)+bB(g)?cC(g)+dD(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图,下列叙述正确的是( )| A. | 化学方程式中a+b>c+d | |
| B. | 达平衡后,加入催化剂则C%增大 | |
| C. | 达平衡后,若升温,平衡逆向移动 | |
| D. | 其他条件不变,在不同温度达平衡后,C在T1时的反应速率大于T2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.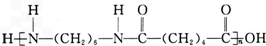 +(2n-1)H2O.
+(2n-1)H2O.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com