

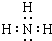 ������鷽��Ϊʹʪ��ĺ�ɫʯ����ֽ�������ʴ�Ϊ��
������鷽��Ϊʹʪ��ĺ�ɫʯ����ֽ�������ʴ�Ϊ��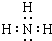 ��ʹʪ��ĺ�ɫʯ����ֽ������
��ʹʪ��ĺ�ɫʯ����ֽ������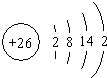 ����λ��Ԫ�����ڱ��������ڵڢ����壬�ʴ�Ϊ���������ڵڢ����壻
����λ��Ԫ�����ڱ��������ڵڢ����壬�ʴ�Ϊ���������ڵڢ����壻
| ||
| ||
| 2b |
| a |
| 1 |
| 2 |
| 2b |
| a |
| 1 |
| 2 |
| 2b |
| a |


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 �����ͼװ��̽��HCl��Һ�������������ڵ糡�е����Ǩ�����ʣ���֪��Cd�Ľ�����Դ���Cu���������£��ڴ�ֱ�IJ���ϸ���ڣ��ȷ�CdCl2��Һ����ɫ����Ȼ��С�ķ���HCl��Һ����aa�䴦�γ������Ľ��森ͨ��ɹ۲쵽�������滺�������ƶ�������˵������ȷ���ǣ�������
�����ͼװ��̽��HCl��Һ�������������ڵ糡�е����Ǩ�����ʣ���֪��Cd�Ľ�����Դ���Cu���������£��ڴ�ֱ�IJ���ϸ���ڣ��ȷ�CdCl2��Һ����ɫ����Ȼ��С�ķ���HCl��Һ����aa�䴦�γ������Ľ��森ͨ��ɹ۲쵽�������滺�������ƶ�������˵������ȷ���ǣ�������| A��ͨ��ɹ۲쵽�������滺�������ƶ���ԭ����Cd2+��Pt�缫Ǩ�ƵĽ�� |
| B��װ����Pt�缫������pH���� |
| C��һ��ʱ���ڣ����ͨ��HCl��Һijһ������ܵ���Ϊ5.0C�����H+��Ǩ�Ƶĵ���Ϊ4.1C��˵����HCl��Һ��H+��Ǩ������Լ��Cl-��4.6�� |
| D�������Դ���������ӣ����¶˲�������Cl2��ʹ���治��������ʵ��ʧ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����³�ѹ�£�5.6g N2��CO������������е�ԭ������Ϊ0.4NA |
| B��0.1mol Na2O2����������������Ϊ0.2NA |
| C����0.2mol FeCl3ˮ���Ƴɽ��壬���ý���������Ϊ0.2NA |
| D����״���£�2.24L H2O�к��е���ԭ����ĿΪ0.1NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| ���� | Al3+ | Fe3+ | Ni2+ |
| pH | 5.2 | 4.1 | 9.7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ʹʯ����Һ������Һ�У�I-��MnO4-��NO3-��Na+ |
| B�����д���Fe3+����Һ��NH4+��HCO3-��SO42-��AlO2- |
| C��ˮ�����C��H+��=1.0��10-12mol/L ����Һ��Cl-��Na+��ClO-��NH4+ |
| D������������Һ��Cu2+��Fe3+��SO42-��NO3- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�������̪��Һ�Ժ�ɫ����Һ�У�K+��Na+��Cu2+��SO42- |
| B���������NaOH��Һ������ϡH2SO4ʱ�����ܲ�����ɫ��������Һ��Al3+��Ba2+��Cl-��HCO3- |
| C��ˮ���������c��H+��=10-13mol?L-1����Һ�У�Na+��Cl-��NO3-��SO42- |
| D��0.1mol?L-1HNO3��Һ�У�Mg2+��NH4+��Fe2+��Cl- |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com