
 =2Cr��OH��3��+3O2��+2H2O��
=2Cr��OH��3��+3O2��+2H2O������ ��1����H2O2ֻ�������¹���H2O2-��O2��֪�����øù�����OԪ�صĻ��ϼ���-1�����ߵ�0��������
��2��������������ԭ��Ӧ������Ԫ�صĻ��ϼ۽�����������
��3����ʧȥ���ӵ�Ԫ��ָ��õ����ӵ�Ԫ�أ����������ת�Ƶ��������õ����ŷ��������ת�Ƶķ������Ŀ��
��4���ɷ�Ӧ��֪����3mol����ת��6mol���ӣ��Դ������㣻
��5������������ԭ��Ӧ�л�ԭ���Ļ�ԭ�Դ��ڻ�ԭ����Ļ�ԭ�ԣ�����������Һ�л�ԭ��ǿ����˳����SO2��I-��H2O2��Fe2+��Cl-���жϷ�Ӧ�ܷ�����
��� �⣺��1������ϢH2O2-��O2�п�֪��OԪ�صĻ��ϼ���-1�����ߵ�0����H2O2Ϊ��ԭ�����ʴ�Ϊ��H2O2��
��2��������������ԭ��Ӧ����Ԫ�ػ��ϼ۽��͵�����Ϊ����������CrԪ�صĻ��ϼ۽��ͣ�����ԭ��Ӧ�Ĺ���ΪH2CrO4��Cr��OH��3���ʴ�Ϊ��H2CrO4��Cr��OH��3��
��3���÷�Ӧ��OԪ��ʧ���ӣ�CrԪ�صõ����ӣ�2molH2CrO4��Ӧת�Ƶ���Ϊ2mol����6-3��=6mol�����õ����ŷ��������ת�Ƶķ������ĿΪ =2Cr��OH��3��+3O2��+2H2O��
=2Cr��OH��3��+3O2��+2H2O��
�ʴ�Ϊ�� =2Cr��OH��3��+3O2��+2H2O��
=2Cr��OH��3��+3O2��+2H2O��
��4����2H2CrO4+3H2O2�T2Cr��OH��3��+3O2��+2H2O��֪������3mol����ת��6mol���ӣ���ת����0.3mol���ӣ����������������ʵ���Ϊ$\frac{0.3}{6}$mol=0.15mol��
���ڱ�״�������Ϊ0.15mol��22.4L/mol=3.36L���ʴ�Ϊ��3.36L��
��5��A����÷�Ӧ��SԪ�صĻ��ϼ����ߣ�FeԪ�صĻ��ϼ۽��ͣ���SO2Ϊ��ԭ������ԭ��ǿ��ΪSO2��Fe2+������֪�Ļ�ԭ��ǿ��һ�£��ܷ�������A��ѡ��
B����÷�Ӧ��SԪ�صĻ��ϼ����ߣ�IԪ�صĻ��ϼ۽��ͣ���SO2Ϊ��ԭ������ԭ��ǿ��ΪSO2��I-������֪�Ļ�ԭ��ǿ��һ�£��ܷ�������B��ѡ��
C����÷�Ӧ��OԪ�صĻ��ϼ����ߣ�SԪ�صĻ��ϼ۽��ͣ���H2O2Ϊ��ԭ������ԭ��ǿ��ΪH2O2��SO2������֪�Ļ�ԭ��ǿ����һ�£���Ӧ���ܷ�������Cѡ��
D����÷�Ӧ��FeԪ�صĻ��ϼ۽��ͣ�IԪ�صĻ��ϼ����ߣ���I-Ϊ��ԭ������ԭ��ǿ��ΪI-��Fe2+������֪�Ļ�ԭ��ǿ��һ�£��ܷ�������D��ѡ��
��ѡC��
���� ���⿼��������ԭ��Ӧ����ȷ�������ⷢ���ķ�Ӧ��������ԭ��Ӧ�м���Ԫ�صĻ��ϼ���������Ԫ�صĻ��ϼ۽����������ǽ��Ĺؼ���Ȼ�����û��ϼ۱仯��������ӵ�ת�Ƽ��ɣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
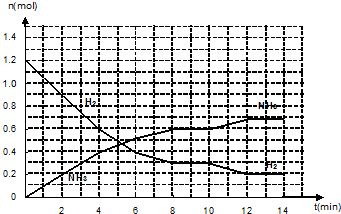
| A�� | ���е��Ȼ�ѧ����ʽΪ2C��g��?A��g��+3B��g������H=+4Q2/3kJ/mol | |
| B�� | ��Ӧ�ﵽƽ��ǰ������ʼ����v������v��������ʼ����v������v�� | |
| C�� | �ڸ������£���Ӧ2C��g��?A��g��+3B��g����ƽ�ⳣ��Ϊ9��1.52��mol/L��2 | |
| D�� | ����C��ת����Ϊ25% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ̼��������ᷴӦ��CO32-+2H+=H2O+CO2�� | |
| B�� | ϡH2SO4�����۷�Ӧ��2Fe+6H+=2Fe3++3H2�� | |
| C�� | ����������Һ��ϡH2SO4��Ӧ��Ba2++SO42-=BaSO4�� | |
| D�� | ��������������������Fe��OH��3+3H+=Fe3++3H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����£����ý�̿��ʯӢɰ��SiO2����ȡ�ߴ��ȹ� | |
| B�� | CO2������һ�������¿��Եõ����ʯ��̼���ƣ���Ӧ���������ͻ�ԭ��֮����4��1 | |
| C�� | �øߴ��ȹ���Ϊ���ά����Ҫ���� | |
| D�� | �ִ���սͨ�����Һ��SiCl4������ˮ�⣩��Һ���ɲ�����Ļ������Ҫ�ɷ���NH4Cl |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
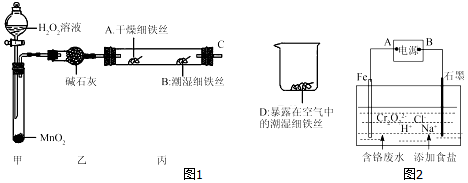
| A�� | ��������������Һʱ�����ȱ��ò��������裬ֱ��Һ��ȫ������ | |
| B�� | �������ʱ��Ӧ���¶ȼƲ���������ƿ�ڻ����Һ�� | |
| C�� | ��ȡ����ʱ��Ӧѡ���л���ȡ��������ȡ�����ܶȱ����ˮ�� | |
| D�� | ��Һ����ʱ����Һ©�����²�Һ����¿ڷų����ϲ�Һ����Ͽڵ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ڢܢ� | B�� | �ۢݢ� | C�� | �٢ڢ� | D�� | �٢ۢ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com