
| A. | 它可使酸性高锰酸钾溶液褪色 | B. | 它能使溴水褪色 | ||
| C. | 它可与银氨溶液反应 | D. | 若催化加氢,最终产物是 C10H20O |
分析 (CH3)2C=CHCH2CH2C=CH(CH3)CHO中含双键、-CHO,结合烯烃和醛的性质来解答.
解答 解:A.含有醛基和碳碳双键,都可与酸性高锰酸钾溶液发生氧化还原反应,故A正确;
B.碳碳双键可与溴发生加成反应,醛基可被溴水氧化,故B正确;
C.含有醛基,可发生银镜反应,故C正确;
D.双键、-CHO均与氢气发生加成反应生成饱和醇,则若催化加氢,最终产物是C10H22O,故D错误;
故选D.
点评 本题考查有机物的结构和性质,侧重于有机物化合物知识的综合应用,为高考常见题型,注意把握有机物官能团的性质,为解答该类题目的关键,易错点为A,注意分子中能与氢气发生加成反应的种类和数目,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | K-、Ba2+、NO3-、SO32- | B. | NH4+、Al3+、Cl-、SO42- | ||
| C. | K Na2+[Al(OH)4]-、SO42- | D. | Na+、K+、SO42-、Br- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 用浓硫酸和Cu制取SO2 | B. | 用浓盐酸和MnO2制取Cl2 | ||
| C. | 用过氧化氢和二氧化锰制取O2 | D. | 用NH4C1溶液和Ca(OH)2制取NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④ | B. | ①④⑥ | C. | ①④⑤ | D. | ②③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
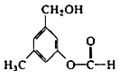 在一定条件下可以发生银镜反应
在一定条件下可以发生银镜反应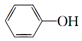 +CO32-→
+CO32-→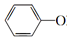 +HCO3-
+HCO3-| A. | 3 | B. | 4 | C. | 5 | D. | 6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 2015年,中国科学家屠哟哟因发现治疗疟疾的药物青蒿素获得了诺贝尔奖.青蒿素结构简式如图所示.己知一个碳原子上连有4个不同的原子或基团,该碳原子称了“手性碳原子”.下列有关青蒿素的说法不正确的是( )
2015年,中国科学家屠哟哟因发现治疗疟疾的药物青蒿素获得了诺贝尔奖.青蒿素结构简式如图所示.己知一个碳原子上连有4个不同的原子或基团,该碳原子称了“手性碳原子”.下列有关青蒿素的说法不正确的是( )| A. | 青蒿素分子有6个手性碳原子 | |
| B. | 青蒿素的化学式为:C15H22O5 | |
| C. | 青蒿素在一定条件下能与NaOH溶液反应,且有氧化性 | |
| D. | 青蒿素难溶于水,提取的方法是用有机溶剂萃取后蒸馏 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在已知碱金属元素中具有最大的原子半径 | |
| B. | 其氧化物对应的水化物是极强的碱 | |
| C. | 在空气中燃烧时生成氧化物Fr2O | |
| D. | 在已知碱金属元素单质中熔点最低 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com