
某混合气体由CH4和CO组成,在标准状况下测得密度为1g/L,则该混合气体中CH4和CO的物质的量之比为
A.11 B 12 C 23 D、78
科目:高中化学 来源: 题型:
氧化还原反应广泛应用于金属的冶炼。下列说法不正确的是( )
A.电解熔融氯化钠制取金属钠的反应中,钠离子被还原,氯离子被氧化
B.湿法炼铜与火法炼铜的反应中,铜元素都发生还原反应
C.用磁铁矿炼铁的反应中,1 mol Fe3O4被CO还原成Fe,转移9 mol e-
D.铝热法还原铁的反应中,放出的热量能使铁熔化
查看答案和解析>>
科目:高中化学 来源: 题型:
可逆反应A(g)+B C(g)+D,A和C均为无色气体,B和D的聚集状态未知,当反应到
C(g)+D,A和C均为无色气体,B和D的聚集状态未知,当反应到
达平衡时,下列叙述不正确的是
A.若保持恒容,充入C气体后混合气体颜色加深,则说明B是有颜色的气体
B.若升高温度,发现C的物质的量减少,则说明正反应为放热反应
C.若压缩容器,平衡不移动,则说明B和D一定都是气体
D.保持恒容,到达平衡后继续充入A会使B的转化率增大,A的转化率减少
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数,下列叙述正确的是
A.标准状况下,22.4L H2O含有的分子数为 NA
B.常温常压下,1.06g Na2CO3溶于水形成的溶液中含有Na+离子数为0.02 NA
C.通常状况下,NA 个CO2分子占有的体积为22.4L
D.物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl- 个数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
用10 mL的0.1 mol·L-1 BaCl2溶液恰好可使相同体积的硫酸铁(Fe2(SO4)3)、硫酸锌(ZnSO4)和硫酸钾(K2SO4)三种溶液中的硫酸根离子完全转化为硫酸钡沉淀,则三种硫酸盐溶液的物质的量浓度之比是
A.3∶2∶2 B 1∶2∶3 C 1∶3∶3 D 3∶1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
质量分数为n的硫酸溶液,其物质的量浓度a mol/L为,加热蒸发水使其质量分数变为2n,此时,该溶液中的物质的量浓度为b mol/L,则与的关系正确的是
A.b=2a B.a=2b C.b﹥2a D.b﹤2a
查看答案和解析>>
科目:高中化学 来源: 题型:
在标准状况下,有一刚性密闭容器,被一可以自由滑动的活塞分成两个密闭的反应器。左侧充入等物质的量的氢气和氧气,右侧充入一氧化碳和氧气的混合气体。同时引燃左右两侧的混合气,反应后恢复到标准状况,反应前后活塞位置如下图所示,则右侧混合气体中一氧化碳和氧气的物质的量之比可能是(液态水的体积忽略不计)
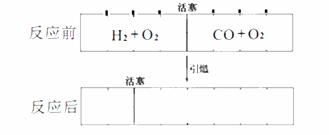
查看答案和解析>>
科目:高中化学 来源: 题型:
在Na2S溶液中下列关系不正确的是 ( )
A.c(Na+) =2c( HS-) +2c(S2-) +2c(H2S) B. c(Na+) +c(H+)=c(OH-)+c(HS-)+ 2c(S2-)
C.c(Na+) > c(S2-) >c(OH-)>c(HS-) D.c(OH-)=c(HS-)+c(H+)+ c(H2S)
查看答案和解析>>
科目:高中化学 来源: 题型:
请订正下面的错误。
(1)硫在足量氧气中燃烧:2S+3O2===2SO3。
________________________________________________________________________。
(2)AlCl3溶液呈酸性的原因:Al3++3H2O===Al(OH)3↓+3H+。
________________________________________________________________________。
(3)NaOH溶液与稀硫酸反应的离子方程式:2H++2OH-===2H2O。
________________________________________________________________________。
(4)工业合成氨反应:N2+3H2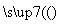 2NH3。
2NH3。
___________________________________ _____________________________________。
_____________________________________。
(5)工业上用氧化铝为原料制备金属铝:2Al2O3 4Al+3O2↑。
4Al+3O2↑。
________________________________________________________________________。
(6)NH4Cl溶液和NaOH溶液加热反应:NH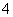 +OH-NH3·H2O。
+OH-NH3·H2O。
________________________________________________________________________。
(7)钢铁吸氧腐蚀,正极的电极反应:O2+2H2O===4OH-+4e-。
________________________________________________________________________。
(8)实验室制取氯气的离子方程式:MnO2+4HCl===MnCl2+Cl2↑+2H2O。
________________________________________________________________________。
(9)铜与浓硝酸反应:Cu+4HNO3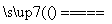 Cu(NO3)2+2NO2↑+2H2O。
Cu(NO3)2+2NO2↑+2H2O。
________________________________________________________________________。
(10)1 g肼气体燃烧生成氮气和水蒸气,放出热量16.7 kJ。反应的热化学方程式:
N2H4+O2===N2+2H2O ΔH=+16.7 kJ。
________________________________________________________________________。
(11)用惰性电极电解硫酸铜溶液的离子方程式
2Cu2++4OH-===2Cu+O2↑+2H2O。
________________________________________________________________________。
(12)Ba(OH)2溶液与稀硫酸反应的离子方程式:
Ba2++OH-+H++SO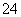 ===BaSO4↓+H2O。
===BaSO4↓+H2O。
________________________________________________________________________。
(13)铝—海水电池的负极反应式:Al-3e-+4OH-===[Al(OH)4]-。
________________________________________________________________________。
(14)碳酸氢钠在水中电离:NaHCO3 Na++H++CO
Na++H++CO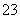 。
。
________________________________________________________________________。
(15)HCO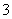 的水解方程式:HCO
的水解方程式:HCO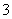 +H2O
+H2O H3O++CO
H3O++CO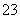 。
。
________________________________________________________________________。
(16)NaHSO4熔化时电离方程式:NaHSO4===Na++H++SO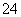 。
。
________________________________________________________________________。
(17)NH4Cl溶液呈酸性的原因:NH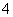 +H2O
+H2O NH4OH+H+。
NH4OH+H+。
________________________________________________________________________。
(18)铜与浓硫酸反应:Cu+2H2SO4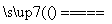 CuSO4+SO2↑+2H2O。
CuSO4+SO2↑+2H2O。
__________________________________________________________ ______________。
______________。
(19)NH4Cl固体和消石灰加热制NH3:2NH4Cl+Ca(OH)2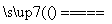 CaCl2+2NH3↑+H2O。
CaCl2+2NH3↑+H2O。
________________________________________________________________________。
(20)实验室制Cl2:4HCl(浓)+MnO2===MnCl2+Cl2↑+2H2O。
_______________________________________________________ _________________。
_________________。
(21)实验室利用H2O2分解制O2:2H2O2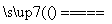 2H2O+O2↑。
2H2O+O2↑。
____ ____________________________________________________________________。
____________________________________________________________________。
(22)1 g氢气在足量氧气中燃烧生成液态水时,放出热量142.9 kJ,热化学方程式可表示为
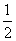 H2(g)+
H2(g)+ O2(g)
O2(g)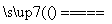
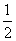 H2O(l) ΔH=-142.9 kJ。
H2O(l) ΔH=-142.9 kJ。
________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com