
用惰性电极电解一定量的硫酸铜溶液,实验装置如图①。电解过程中的实验数据如图②,横坐标表示电解过程中转移电子的物质的量,纵坐标表示电解过程中产生气体的总体积(标准状况)。则下列说法正确的是( )
| A.电解过程中,b电极表面先有红色物质析出,后有气泡产生 |
| B.从开始到Q点时收集到的混合气体的平均摩尔质量为17g·mol-1 |
| C.曲线OP段表示H2和O2混合气体的体积变化,曲线PQ段表示O2的体积变化 |
D.a电极上发生的反应方程式为: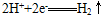 和 和 |
B
解析试题分析:惰性电极电解硫酸铜溶液,阳极始终是OH-放电,生成氧气。阴极先是铜离子放电生成铜,然后是溶液中的氢离子放电生成氢气。根据图①可知b电极是阳极,a电极是阴极,所以a电极表面先有红色物质析出,后有气泡产生,选项A、D不正确;根据图②中课P碘收集到的是0.05mol氧气,Q点收集到的是氢气和和氧气的混合气,其中氧气和氢气都是0.1mol,则混合气的平均摩尔质量为(2+32)g/mol÷2=17g/mol,选项B正确;曲线OP段只生成氧气,C不正确,答案选B。
考点:考查电解原理的应用和有关判断、计算
点评:该题的是中等难度的试题,主要是考查考生对电解原理的熟悉了解程度,旨在考查学生灵活运用基础知识解决实际问题的能力,该题关键是明确电解产物的判断,在判断电解产物时,首先判断阳极电极材料。如果是活性电极,则电极本身失去电子。如果是惰性电极,则溶液中的阴离子失去电子。而阴极是溶液中的阳离子得到电子,所以需要熟练记住常见离子的放电顺序。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 用惰性电极电解一定量的硫酸铜溶液,电解过程中的实验数据如图所示.横坐标表示转移电子的物质的量,纵坐标表示电解过程中产生气体的总体积(标准状况).下列判断正确的是( )
用惰性电极电解一定量的硫酸铜溶液,电解过程中的实验数据如图所示.横坐标表示转移电子的物质的量,纵坐标表示电解过程中产生气体的总体积(标准状况).下列判断正确的是( )查看答案和解析>>
科目:高中化学 来源: 题型:

| A、电解过程中,a电极表面先有红色物质析出,后有气泡产生 | ||||
B、b电极上发生的反应方程式为4OH--4e-
| ||||
| C、曲线O~P段表示H2的体积变化 | ||||
| D、Q点时收集到的混合气体中H2和O2体积比为1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
用惰性电极电解一定量的硫酸铜溶液,通电一段时间后,向电解后的溶液中加入0.1mol
Cu(OH)2固体,恰好能使硫酸铜溶液恢复原来的浓度和质量,则在电解过程中转移的电子的
物质的量为( )
A. 0.2mol B. 0.4mol C. 0.5mol D. 0.6mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com