
【题目】在下列各组的比较中,前者比后者大的是
A.同温度、同浓度的NaCl溶液和氨水的导电能力
B.25℃时,pH均为2的盐酸和CH3COOH溶液中溶质的物质的量浓度
C.25℃时,pH均为2的H2SO4溶液和盐酸中氢离子的物质的量浓度
D.25℃时,pH均为3的盐酸和FeCl3溶液中水的电离程度
【答案】A
【解析】
试题分析:A.同温度、同浓度的NaCl溶液和氨水,氯化钠是强电解质完全电离NaCl=Na++Cl-,电离出的离子浓度等于氯化钠浓度的两倍,而氨水是弱电解质,部分电离,所以电离出的离子小于其浓度的两倍,离子浓度大导电能力强,所以,导电能力前者比后者大,故A正确;B.根据pH=-lgc(H+)公式,pH均为2,H2SO4溶液和盐酸中氢离子的物质的量浓度c(H+)=1×10-2mol/L,盐酸是强酸完全电离,所以,盐酸的物质的量浓度等于1×10-2mol/L,乙酸是弱酸部分电离,它的物质的量的浓度大于1×10-2mol/L,前者小,后者大,故B错误;C.根据pH=-lgc(H+)公式,pH均为2,H2SO4溶液和盐酸中氢离子的物质的量浓度c(H+)=1×10-2mol/L,两者相等,故C错误;D.水的电离方程式:H2O![]() H++OH-,加入酸或碱抑制水的电离,加入能水解的盐促进水的电离,盐酸是强电解质完全电离,三氯化铁是强酸弱碱盐水解,所以前者抑制水的电离,后者促进水的电离,前者小于后者,故D错误;故选A。
H++OH-,加入酸或碱抑制水的电离,加入能水解的盐促进水的电离,盐酸是强电解质完全电离,三氯化铁是强酸弱碱盐水解,所以前者抑制水的电离,后者促进水的电离,前者小于后者,故D错误;故选A。


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案科目:高中化学 来源: 题型:
【题目】下列有关实验装置进行的相应实验,能达到实验目的的是
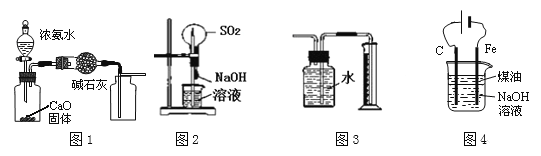
A.用图1装置制取并收集干燥纯净的NH3
B.用图2装置可以完成“喷泉”实验
C.用图3装置直接测量Cu与浓硝酸反应产生的NO2体积
D.用图4装置制备Fe(OH)2并能较长时间观察其颜色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“可燃冰”又称“天然气水合物”,它是在海底的高压、低温的条件下形成的,外观象冰。1体积“可燃冰”可贮载100~200体积的天然气。下面关于“可燃冰”的叙述不正确的是( )
A.“可燃冰”有可能成为人类未来的重要能源
B.“可燃冰”是一种比较洁净的能源
C.“可燃冰”提供了水可能变成油的例证
D.“可燃冰”的主要成分是甲烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组同学用如图所示装置研究电化学原理。下列关于该原电池的说法不正确的是
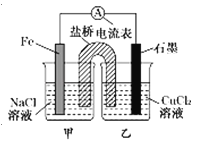
A.原电池的总反应为Fe+Cu2+═Fe2++Cu
B.盐桥中是KNO3溶液,则盐桥中NO3﹣移向乙烧杯
C.其他条件不变,若将CuCl2溶液换为NH4Cl溶液,石墨电极反应式为2H++2e﹣═H2↑
D.反应前,电极质量相等,一段时间后,两电极质量相差12g,导线中通过0.2mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物甲分子式为 CllH14O2,在酸性条件下水解生成乙和丙,丙遇 FeC13溶液显色,丙的相对分子质量比乙大 20,甲的结构有
A. 3种 B. 4种 C. 8种 D. 6种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】温度为500℃时,反应4NH3+5O2![]() 4NO+6H2O在5L的密闭容器中进行,30秒后NH3的物质的量减少了0.6mol,则此反应的速率v(x)为
4NO+6H2O在5L的密闭容器中进行,30秒后NH3的物质的量减少了0.6mol,则此反应的速率v(x)为
A. v(O2)="0.3" mol·L-1·s-1 B. v(NO)=0.24mol·L-1·s-1
C. v(NH3)="0.12" mol·L-1·s-1 D. v(H2O)=0.36mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有BaCl2和NaCl的混合溶液a L,将它平均分成两份。一份滴加稀硫酸,使Ba2+完全沉淀;另一份滴加AgNO3溶液,使Cl-完全沉淀。反应中消耗x mol H2SO4、y mol AgNO3。据此得知原混合溶液中的Na+浓度(mol·L-1)为( )
A.(y-2x)/a B.(y-x)/a
C.(2y-2x)/a D.( 2y-4x)/a
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com