

分析 反应①为石英砂和焦炭生成粗硅和一氧化碳的反应:SiO2+2C$\frac{\underline{\;1373-1623K\;}}{\;}$Si+2CO↑,属于置换反应;反应②是Si+3HCl$\frac{\underline{\;523-527\;}}{\;}$SiHCl3+H2,属于置换反应;反应③是SiHCl3+H2$\frac{\underline{\;1357K\;}}{\;}$Si+3HCl,属于置换反应;反应④为特定条件下的反应:CO+H2O(g)$\frac{\underline{\;催化剂1073K\;}}{\;}$CO2+H2,不属于置换反应.A、B、C分别为CO、CO2、HCl,其中CO2是温室气体,是节能减排的目标气体,CO2和HCl通入W(硅酸钠)溶液中能够生成白色沉淀(硅酸).
(1)置换反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应;
(2)反应③是SiHCl3被氢气还原得到硅和氯化氢;
(3)二氧化硅与碳酸钠高温反应生成硅酸钠;
(4)A、B、C分别为CO、CO2、HCl,化合物W为硅酸钠;
(5)碳和水反应生成一氧化碳和氢气,一氧化碳和水反应生成二氧化碳和氢气,二氧化碳能和氢氧化钙反应生成碳酸钙.
解答 解:(1)置换反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,①②③属于置换反应,故答案为:①②③;
(2)反应③是SiHCl3被氢气还原得到硅和氯化氢,反应的化学方程式为SiHCl3+H2$\frac{\underline{\;1357K\;}}{\;}$Si+3HCl,故答案为:SiHCl3+H2$\frac{\underline{\;1357K\;}}{\;}$Si+3HCl;
(3)二氧化硅与碳酸钠高温反应生成硅酸钠,反应方程式为SiO2+Na2CO3$\frac{\underline{\;1373-1623K\;}}{\;}$Na2SiO3+CO2↑,故答案为:SiO2+Na2CO3$\frac{\underline{\;1373-1623K\;}}{\;}$Na2SiO3+CO2↑;
(4)A、B、C分别为CO、CO2、HCl,作为减排目标的一种气体是CO2,化合物W为硅酸钠,能与W反应生成沉淀的是CO2和HCl,
故答案为:CO2;CO2和HCl;
(5)碳和水反应生成一氧化碳和氢气:C+H2O(g)$\frac{\underline{\;高温\;}}{\;}$CO+H2,一氧化碳和水反应生成二氧化碳和氢气:CO+H2O(g)$\frac{\underline{\;催化剂1073K\;}}{\;}$CO2+H2,二氧化碳能和氢氧化钙反应生成碳酸钙:CO2+Ca(OH)2═CaCO3↓+H2O,
故答案为:CO+H2O(g)$\frac{\underline{\;催化剂1073K\;}}{\;}$CO2+H2、CO2+Ca(OH)2═CaCO3↓+H2O.
点评 本题考查无机物的推断,主要是物质转化关系,物质制备流程分析判断,明确各物质的成分是解题的关键,题目难度中等.


科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
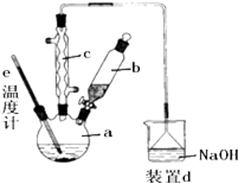 溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如图:按下列合成步骤回答问题:
溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如图:按下列合成步骤回答问题:| 苯 | 溴 | 溴苯 | |
| 密度/g•cm-3 | 0.88 | 3.10 | 1.50 |
| 沸点/°C | 80 | 59 | 156 |
| 水中溶解度 | 微溶 | 微溶[来 | 微溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上期中化学试卷(解析版) 题型:选择题
下列有关说法中,不正确的是
A.“光化学烟雾”“硝酸型酸雨”的形成都与氮氧化合物有关
B.根据分散质微粒直径大小可以将分散系分为溶液、胶体和浊液
C.SiO2可用于制造光导纤维,其性质稳定,不溶于强酸、强碱
D.焰火的五彩缤纷是某些金属元素的性质的表现
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com