
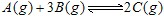 达到平衡的标志的是:
达到平衡的标志的是:科目:高中化学 来源:不详 题型:单选题
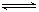 CO2(g)+H2(g) ΔH=-43kJ/mol,在850℃时,K=1,今在某密闭容器中充入1.0molCO、3.0molH2O、1.0molCO2、xmolH2,下列说法不正确的是( )
CO2(g)+H2(g) ΔH=-43kJ/mol,在850℃时,K=1,今在某密闭容器中充入1.0molCO、3.0molH2O、1.0molCO2、xmolH2,下列说法不正确的是( )A.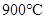 ,该反应的平衡常数 ,该反应的平衡常数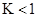 |
B.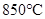 达到平衡时,通入CO,CO转化率将增大 达到平衡时,通入CO,CO转化率将增大 |
C.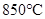 时,若 时,若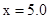 ,则起始时平衡向逆反应方向移动 ,则起始时平衡向逆反应方向移动 |
D.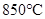 时,若要使上述反应开始时向正反应方向进行,则 时,若要使上述反应开始时向正反应方向进行,则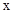 应满足 应满足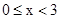 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
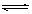 H+ + In-(黄色)△H>0对上述平衡解释不正确的是
H+ + In-(黄色)△H>0对上述平衡解释不正确的是| A.升高温度平衡向正方向移动 |
| B.加入盐酸后平衡向逆方向移动,溶液显红色 |
| C.加入NaOH溶液后平衡向正方向移动,溶液显黄色 |
| D.加入NaHSO4溶液后平衡向正方向移动,溶液显黄色 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2C(g),可以判断达到化学平衡状态的是
2C(g),可以判断达到化学平衡状态的是| A.体系压强不变 | B.单位时间消耗n molA,同时生成2nmolC |
| C.A的转化率不变 | D.容器内气体密度不变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2SO3(g)(正反应放热)反应过程中SO2、O2、SO3物质的量变化如图所示:回答下列问题:
2SO3(g)(正反应放热)反应过程中SO2、O2、SO3物质的量变化如图所示:回答下列问题: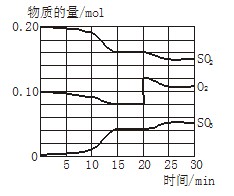
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 Cl2(g) + CO(g) △H =" +" 108 KJ·mol-1。反应体系达到平衡后,各物质的浓度在不同条件下的变化状况如大图(每次仅改变一个条件):
Cl2(g) + CO(g) △H =" +" 108 KJ·mol-1。反应体系达到平衡后,各物质的浓度在不同条件下的变化状况如大图(每次仅改变一个条件):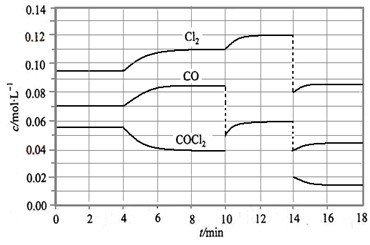
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Q1+ Q2 + Q3 | B.0.5 Q3-Q2+2Q1 |
| C.0.5 Q3+ Q2-2Q1 | D.0.5(Q1+Q2+Q3) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 Na2S(s)+4H2O(g),△H<0,在恒温恒容时回答以下问题:
Na2S(s)+4H2O(g),△H<0,在恒温恒容时回答以下问题: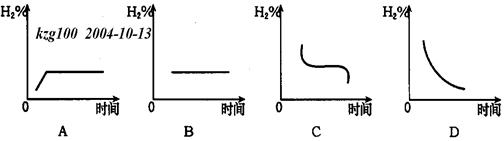
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
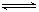 SO3(g)+NO(g)的平衡常数K=0.24,下列说法正确的是
SO3(g)+NO(g)的平衡常数K=0.24,下列说法正确的是A.该温度下反应2SO2(g)+2NO2(g)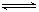 2SO3(g)+2NO(g) 的平衡常数为0.48 2SO3(g)+2NO(g) 的平衡常数为0.48 |
| B.若该反应ΔH <0,则升高温度化学平衡常数K减小 |
| C.若升高温度,逆反应速率减小 |
| D.改变条件使平衡正向移动,则平衡时n(NO2)/n(NO)一定比原平衡小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com