

分析 (1)烯烃A与H2发生加成反应后得到的产物是CH3CH(CH3)2,则A的结构简式为CH2=C(CH3)2,可与溴发生加成反应;
(2)烯烃A被酸性高锰酸钾溶液氧化的最终产物之一B为(CH3)2C=O,B与HCN发生加成反应;
(3)相邻C上均有H时去掉H可形成烯烃,相邻C上均有2个H时去掉H可形成炔烃.
解答 解:(1)烯烃A与H2发生加成反应后得到的产物是CH3CH(CH3)2,则A的结构简式为CH2=C(CH3)2,与溴发生加成反应的方程式为CH2=C(CH3)2+Br2→CH2BrCBr(CH3)2,
故答案为:CH2=C(CH3)2+Br2→CH2BrCBr(CH3)2 ;
(2)烯烃A被酸性高锰酸钾溶液氧化的最终产物之一B为(CH3)2C=O,B与HCN发生加成反应,则反应为(CH3)2C=O+HCN$\stackrel{催化剂}{→}$(CH3)2C(OH)CN,
故答案为:(CH3)2C=O+HCN$\stackrel{催化剂}{→}$(CH3)2C(OH)CN;
(3)相邻C上均有H时去掉H可形成烯烃,则除与3个甲基相连的C不能形成烯烃,共5种单烯烃;相邻C上均有2个H时去掉H可形成炔烃,只有最左侧可形成炔烃,共1种,
故答案为:5;1.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重分析与应用能力的考查,注意烯烃的性质,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 金刚石和SiO2 | B. | CO2和SiO2 | C. | NaCl和 HCl | D. | 钠和KCl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
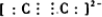 ,其中α键和π键数目之比为1:2.
,其中α键和π键数目之比为1:2.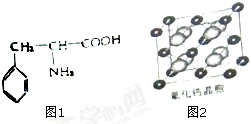
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{a(A-N+3)}{A+3}$mol | B. | $\frac{a(A-N+8)}{A+16}$mol | ||
| C. | $\frac{a(2A-2N+40)}{2A+90}$mol | D. | $\frac{2A-2N+24}{2A+54}$mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
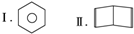
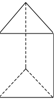 的立体结构,该结构的二氯代物有3种.
的立体结构,该结构的二氯代物有3种. ,该结构简式不能解释萘的下列A事实(填编号).
,该结构简式不能解释萘的下列A事实(填编号).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
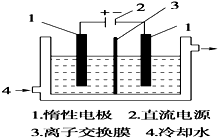 碘被称为“智力元素”,科学合理地补充碘可防止碘缺乏病.碘酸钾(KIO3)是国家规定的食盐加碘剂,它的晶体为白色,可溶于水.碘酸钾在酸性介质中与过氧化氢或碘化物作用均生成单质碘.以碘为原料,通过电解制备碘酸钾的实验装置如图所示.
碘被称为“智力元素”,科学合理地补充碘可防止碘缺乏病.碘酸钾(KIO3)是国家规定的食盐加碘剂,它的晶体为白色,可溶于水.碘酸钾在酸性介质中与过氧化氢或碘化物作用均生成单质碘.以碘为原料,通过电解制备碘酸钾的实验装置如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该物质与乙炔互为同系物 | |
| B. | 能使酸性高锰酸钾溶液褪色 | |
| C. | 不能发生加聚反应 | |
| D. | 可由乙炔和含氮化合物通过取代反应制得 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com