
| A、Fe在常温下可与浓硝酸、稀硝酸、浓硫酸剧烈反应 |
| B、Na久置于空气中,可以与空气中的有关物质发生反应,最终生成Na2CO3粉末 |
| C、Si、Cl2 均能和烧碱溶液发生氧化还原反应,且都既做氧化剂又做还原剂 |
| D、因为碳酸、氨水能够导电,所以液氨、二氧化碳都为电解质 |
| ||


科目:高中化学 来源: 题型:
| 物质 | A | B | C | D |
| X | CaO | BaCl2 | Cu(NO3)2 | K2SO4 |
| Y | CaCl2 | Ba(NO3)2 | Cu(OH)2 | KCl |
| Z | CaCO3 | BaCO3 | CuSO4 | KNO3 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钠钾合金可用于快中子反应堆作热交换剂 |
| B、镁燃烧发出耀眼的白光,常用于制造信号弹和焰火 |
| C、盛浓硫酸的试剂瓶敞口放置在空气中,质量增大,体现了浓硫酸的脱水性 |
| D、铜化学性质不活泼,故古代用作铸币材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铜在冷的浓硫酸中会钝化,所以把铜片放入冷的浓硫酸中无明显现象 |
| B、向FeCl2溶液中加入NaOH溶液,产生的白色沉淀在空气中马上变成红褐色 |
| C、NaOH溶液和AlCl3溶液相互滴加,现象不同 |
| D、分别 蘸有氨水和硝酸的玻璃棒相互靠近,会产生大量白烟 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaHCO3的热稳定性大于Na2CO3 |
| B、FeCl3溶液能与铜反应,故可用于蚀刻印刷线路版 |
| C、Mg和Fe在一定条件下与水反应都生成氢气和对应的碱 |
| D、由于铝在空气中不会锈蚀,故铝制品的使用寿命都很长 |
查看答案和解析>>
科目:高中化学 来源: 题型:
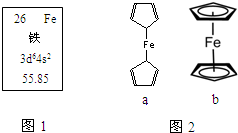 铁及其化合物在生产、生活中存在广泛用途,完成下列填空.
铁及其化合物在生产、生活中存在广泛用途,完成下列填空.查看答案和解析>>
科目:高中化学 来源: 题型:

| 充电 |
| 放电 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 12 |
| 17 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com