
����Ŀ�����ͷ������������������а�������Ҫ�Ľ�ɫ�����ݴ��ͷӵĸ�������ʻش��������⡣
��1�������������ڴ��������
��2��˾���ƺ�ݳ�ʱ�ɼ�������������壬�����õĻ�ѧ��Ӧ���£�
2CrO3(��ɫ)��3C2H5OH��3H2SO4=Cr2(SO4)3(��ɫ)��3CH3CHO��6H2O
����������ɷ��� �� ������Ӧ�е��������� �� ��ԭ������
��3��300����ǰ��������ѧ�Ҳ����������������ûʳ�������ɫ��Ӧ�����ɴ˷���������īˮ��ûʳ����Ľṹ��ʽΪ��  ��ûʳ��������īˮ��Ҫ�����ˣ� ������������(�����)��
��ûʳ��������īˮ��Ҫ�����ˣ� ������������(�����)��
A.��
B.��
C.��֬
D.����
���𰸡�
��1���٢ڢۢܢݢ�
��2��C2H5OH��CrO3��C2H5OH
��3��B
��������(1)�ǻ��������������ϵ�̼ԭ�������Ļ�����Ϊ�����ǻ�ֱ�����ڱ����ϵĻ�����Ϊ�ӣ���ˣ������ڷӣ��������Ϊ����(2)2CrO3(��ɫ)��3C2H5OH��3H2SO4=Cr2(SO4)3(��ɫ)��3CH3CHO��6H2O����Ӧ��CrO3��C2H5OH����ΪCH3CHO�����Ա�������ΪC2H5OH��������ΪCrO3 �� ��ԭ��ΪC2H5OH��(3)��ûʳ��������īˮ��Ҫ���÷ӵ����ʡ�


 ������ʱͬ����ϰ��ϵ�д�
������ʱͬ����ϰ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ͬʱ�����ȷ��ӣ�Cl2���������ӣ�Cl�D�����ǣ� ��
A. Һ��B. ������ˮC. CaCl2��ҺD. ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������﮼��仯�����ڹ��ý�������;�㷺��ռ����Ҫ��λ��
��1�����Ԫ�����ڱ��е�λ����
��2������֤��﮵Ľ����������Ƶ�ʵ����ʵ��
��3����ͼ����ij���±ˮ����Ҫ��Na+��K+��Li+��Mg2+��Clһ�ȣ����еij�﮹���·��ͼ�� 
�١����γ�þ�����õij�������Ҫ�м�ʽ̼��þ��
�ڡ���ﮡ��͡����γ�þ��ʱ���ô����Ũ�Ȳ����ԭ����
��4���������Ʊ���̼��﮼������Ƶ��������Һ����������ͼ��ʾװ���Ʊ�������ﱣ�
��̼��������ᷴӦ�����ӷ���ʽ��
�ڽ�ϵ缫��Ӧʽ�����Ƶ�LiOH��ԭ����
�۸÷��п�ѭ�����õ������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ȡ1 mol��������������ˮ��ַ�Ӧ������Br2�����ʵ�������˳��������ȷ����(����)
�����
�ڶ����ͷ�
�۰�«��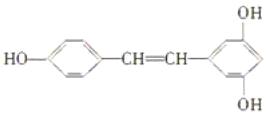
A.2 mol��2 mol��6 mol
B.5 mol��2 mol��6 mol
C.4 mol��2 mol��5 mol
D.3 mol��2 mol��6 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڿ��淴ӦA��g��+3B��g��2C��g��+2D��g�����ڲ�ͬ�����µĻ�ѧ��Ӧ�������£����б�ʾ�ķ�Ӧ���������ǣ�������
A.v��A��=0.5 molL��1min��1
B.v��B��=1.2 molL��1s��1
C.v��D��=0.4 molL��1min��1
D.v��C��=0.1 molL��1s��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����(����)
A. ��������ʯȼ�ϡ���Ȼ�˿���һ����Դ
B. ��Ҫ���Ȳ��ܷ����ķ�Ӧ�������ȷ�Ӧ
C. �Ͽ�1molC��H��Ҫ�ų�һ��������
D. ȼú�����ǽ���ѧ��ֱ��ת��Ϊ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2014��7��31���й����������ӱ�ʡ��չ������������ר�������ж���ǿ�������ϡ�������ij������������Ҫ�ɷ�ΪSiO2��MgO��Al2O3��Fe2O3�ȳɷ֣����շ����еĽ���Ԫ�صĹ���������ͼ��ʾ�� 
��֪�������£����Ͱ�ˮ��pHԼΪ11���������ӳ�������pH���������ʾ��
���� | ������������ʽ��ȫ����ʱ����pH | �������������ȫ�ܽ�ʱ����pH |
Fe3+ | 3.2 | |
A13+ | 5.3 | 11.9 |
Mg2+ | 12.3 |
��1���Լ���Ϊ �� �Լ���Ϊ��
A��AgNO3 B��NaOH C��NH3H2O D��H2SO4
��2������C�Ļ�ѧʽ�� �� ��ҺF�н���Ԫ�صĴ�����ʽΪ��
��3��д������A���Լ��ڷ�Ӧ�Ļ�ѧ����ʽ����F��ͨ�����CO2�����������ӷ���ʽΪ��
��4�������Լ��ڣ�ʵ����ҺD����ҺF��ת�����������Һ��pHΪ ��
A.6
B.10
C.12
D.13
��5��25��ʱ������4������pH������ҺF��c��Mg2+��=5.6��10��10mol/L����������þ��Ksp=��
��6�����һ����Ӧ���漰�������Σ�������ʽ�ε���Һ�и�����Ũ���ɴ�С��˳��Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼʾװ����ȡ������������(�ƾ��Ƶ���ͼ�о�����ȥ)������գ�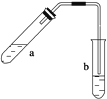
��1���Թ�a����Ҫ����Ũ���ᡢ��������Ҵ���2 mL����ȷ�ļ���˳�����ǣ�
��2��Ϊ��ֹa�е�Һ����ʵ��ʱ�������У��ڼ���ǰӦ��ȡ�Ĵ�ʩ�ǣ�
��3��ʵ���м����Թ�a��Ŀ���ǣ�
��4���Թ�b�м��б���Na2CO3��Һ���������ǣ�
��5����Ӧ���������Թ�b�����á��۲쵽�������ǣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ� ��
A.�������ϵͳ����������Ϊ2����������
B.������������ȥ�����е���ϩ
C.�����м���ˮ������һ��ʱ���Һ�����ɫ��˵��������巢����ȡ����Ӧ
D.���м�������Ȼ�̼��Һ����Һ�ֲ㣬�ϲ�ʳȺ�ɫ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com