
| A. | 钠离子的电子式:Na+ | B. | 二甲醚的分子式:CH3OCH3 | ||
| C. | CO2分子的比例模型: | D. | 16O原子的结构示意图: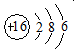 |
分析 A、简单阳离子的电子式是其离子符号本身;
B、表示物质的元素组成的式子为分子式;
C、碳原子半径大于氧原子;
D、16O原子的核内有8个质子,核外有8个电子.
解答 解:A、简单阳离子的电子式是其离子符号本身,故钠离子的电子式为Na+,故A正确;
B、表示物质的元素组成的式子为分子式,故二甲醚的分子式为C2H6O,故B错误;
C、二氧化碳分子中,碳原子的相对体积大于氧原子,其正确的比例模型为: ,故C错误;
,故C错误;
D、16O原子的核内有8个质子,核外有8个电子,故结构示意图为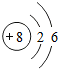 ,故D错误.
,故D错误.
故选A.
点评 本题考查了常见的化学用语,难度不大,应注意在比例模型中原子半径的相对大小,应加强基础的掌握.


 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
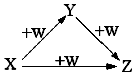 X、Y、Z、W有如图所示的转化关系(反应条件和部分其它反应物省略),则X、Y、Z可能是 ( )
X、Y、Z、W有如图所示的转化关系(反应条件和部分其它反应物省略),则X、Y、Z可能是 ( )| A. | ①②④ | B. | ②④ | C. | ①②③ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+、Ca2+、OH-、HCO3- | B. | NH4+、Br-、Na+、SO42- | ||
| C. | Ag+、H+、SO32-、ClO- | D. | H+、Cl-、Fe2+、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
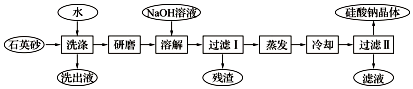
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 纸张电极是该电池的正极 | |
| B. | 锂箔电极发生的电极反应:Li-e-═Li+ | |
| C. | 电池工作时,电子从锂箔电极经导线流向纸张电极,再从纸张电极经电解质溶液流向锂箔电极 | |
| D. | 该电池具有轻型、柔性且可折叠的特点,有望应用于柔性电子器件 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 热稳定性:Na2CO3>NaHCO3 | |
| B. | 相同温度下,0.1mol•L-1盐溶液的pH值:Na2CO3>NaHCO3 | |
| C. | 等质量的碳酸钠和碳酸氢钠分别与足量盐酸反应放出气体的量:Na2CO3<NaHCO3 | |
| D. | 相同温度下,0.1mol•L-1盐溶液分别与0.1mol•L-1HCl反应的剧烈程度:Na2CO3>NaHCO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com