
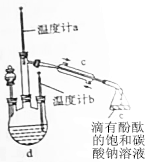
 乙酸丁酯沸点、溶解性如下表.
乙酸丁酯沸点、溶解性如下表.| 物质 | 乙酸 | 1-丁醇 | 乙酸丁酯 | 90%浓硫酸 |
| 沸点 | 117.9℃ | 117.2℃ | 126.3℃ | 338.0℃ |
| 溶解性 | 溶于水和有机溶剂 | 溶于水和有机溶剂 | 微溶于水,溶于有机溶剂 | 与水混溶 |
分析 (1)浓硫酸密度大,应将浓硫酸加入到丁醇中,以防酸液飞溅,乙酸易挥发,冷却后再加入乙酸;乙酸与丁醇在浓硫酸作用下加热反应生成乙酸丁酯和水;
(2)饱和碳酸钠溶液与乙酸反应除去乙酸、溶解丁醇、同时降低乙酸丁酯的溶解度,便于分层;
(3)乙酸丁酯的沸点为126.3℃,所以当温度计a的温度为126.3℃时,收集到的即为乙酸丁酯;
(4)锥形瓶e中收集的乙酸丁酯的中混有乙酸、丁醇,用力振荡,有机混合溶液与碳酸钠溶液充分混合,乙酸与碳酸钠反应生成二氧化碳,同时丁醇溶于碳酸钠溶液,据此判断现象;乙酸乙酯中混有碳酸钠和乙醇,用饱和食盐水萃取碳酸钠,用氯化钙除去少量乙醇,用无水硫酸钠除去少量的水,无水硫酸钠吸水形成硫酸钠结晶水合物;不能选择P2O5、碱石灰和NaOH等固体干燥剂,以防乙酸乙酯在酸性(P2O5遇水生成酸)或碱性条件下水解;
解答 解:(1)浓硫酸密度大于水,且溶于水放出大量热,应该将浓硫酸加入丁醇中,正确操作方法为:将浓H2SO4加入丁醇中,边加边振荡,然后再加入乙酸或先将乙醇与乙酸混合好后再加浓硫酸并在加入过程中不断振荡;酯化反应的本质为酸脱羟基,醇脱氢,乙酸与乙醇在浓硫酸作用下加热发生酯化反应生成乙酸乙酯和水,该反应为可逆反应为:CH3COOH+CH3CH2OH $→_{△}^{浓硫酸}$CH3COOCH2CH3+H2O,
故答案为:先加入丁醇,然后边摇动试管边慢慢加入浓硫酸,再加乙酸;CH3COOH+CH3CH2OH $→_{△}^{浓硫酸}$CH3COOCH2CH3+H2O;
(2)制备乙酸乙酯时常用饱和碳酸钠溶液,目的是中和挥发出来的乙酸,使之转化为乙酸钠溶于水中;溶解挥发出来的乙醇;降低乙酸乙酯在水中的溶解度,便于分层得到酯,所以BC正确,
故答案为:BC;
(3)乙酸丁酯的沸点为126.3℃,所以当温度计a的温度为126.3℃时,收集到的即为乙酸丁酯,
故答案为:a;126.3℃;
(4)碳酸钠水解呈碱性,乙酸乙酯不溶于饱和碳酸钠溶液,密度比水小,有香味,振荡时乙酸和碳酸钠反应而使溶液红色变浅;乙酸乙酯中混有碳酸钠和乙醇,用饱和食盐水萃取碳酸钠,用氯化钙除去少量乙醇,用无水硫酸钠除去少量的水,无水硫酸钠吸水形成硫酸钠结晶水合物;不能选择P2O5、碱石灰和NaOH等固体干燥剂,以防乙酸乙酯在酸性(P2O5遇水生成酸)或碱性条件下水解,
故答案为:在浅红色碳酸钠溶液层上方有无色液体出现,闻到香味,振荡后碳酸钠溶液层红色变浅;碳酸钠、乙醇;B.
点评 本题考查了乙酸乙酯的制取方法,难度中等,注意掌握乙酸乙酯的制备方法及反应原理,明确浓硫酸、饱和碳酸钠溶液在实验中的作用.


 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案科目:高中化学 来源: 题型:多选题
 工业上用CO和H2生产燃料甲醇.一定条件下密闭容器中发生反应,测得数据曲线如图所示(反应混合物均呈气态).下列说法错误的是( )
工业上用CO和H2生产燃料甲醇.一定条件下密闭容器中发生反应,测得数据曲线如图所示(反应混合物均呈气态).下列说法错误的是( )| A. | 反应的化学方程式:CO+2H2?CH3OH | |
| B. | 反应进行至3分钟时,正、逆反应速率相等 | |
| C. | 反应至10分钟,?(CO)=0.075 mol/L•min | |
| D. | 增大压强,平衡正向移动,K增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
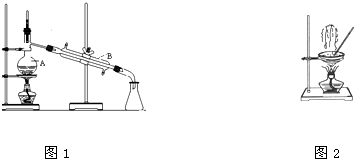 (1)如图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
(1)如图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 化合物A(C4H10O)是一种有机溶剂.A可以发生以下变化:
化合物A(C4H10O)是一种有机溶剂.A可以发生以下变化:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水、硝酸银溶液、稀硝酸 | B. | 水、氢氧化钠溶液、盐酸 | ||
| C. | 水、氢氧化钾溶液、盐酸 | D. | 水、氢氧化钾溶液、硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na投入到足量的盐酸中:2Na+2H2O═2Na++2OH-+H2↑ | |
| B. | 向碳酸氢钠溶液中加入过量氢氧化钙溶液:2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+CO32- | |
| C. | 三氯化铁溶液中加入铜粉:Fe3++Cu═Fe2++Cu2+ | |
| D. | 将氯气通入冷的氢氧化钠溶液中:Cl2+2OH-═Cl-+ClO-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②④ | B. | ②③④ | C. | ①②④ | D. | ②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将金属钠保存在煤油中 | |
| B. | 少量的白磷可保存在水中 | |
| C. | 纯碱溶液用带磨口玻璃瓶塞的试剂瓶保存 | |
| D. | 硝酸银溶液盛放在棕色试剂瓶中 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com