
 一定条件下,CH4与H2O(g)发生反应CH4(g)+H2O(g)?CO(g)+3H2(g),设起始n(H2O)/n(CH4)=Z,在恒压下,平衡时φ(CH4)的体积分数与Z和T(温度)的关系如图所示.下列说法正确的是( )
一定条件下,CH4与H2O(g)发生反应CH4(g)+H2O(g)?CO(g)+3H2(g),设起始n(H2O)/n(CH4)=Z,在恒压下,平衡时φ(CH4)的体积分数与Z和T(温度)的关系如图所示.下列说法正确的是( )| A. | 该反应的焓变△H<0 | |
| B. | 图中Z的大小为a<3<b | |
| C. | 图中X点对应的平衡混合物中$\frac{n({H}_{2}O)}{n(C{H}_{4})}$=3 | |
| D. | 温度不变时,图中X点对应的平衡在加压后φ(CH4)减小 |
分析 由图象可知升高温度,甲烷的体积分数减小,说明升高温度平衡正向移动,则正反应为吸热反应,起始$\frac{n({H}_{2}O)}{n(C{H}_{4})}$=Z,Z越小,说明加入甲烷的物质的量相等水来说越多,含量越大,以此解答该题.
解答 解:A.升高温度,甲烷的体积分数减小,说明升高温度平衡正向移动,则该反应的焓变△H>0,故A错误;
B.起始$\frac{n({H}_{2}O)}{n(C{H}_{4})}$=Z,Z越小,说明甲烷相对越多,达到平衡时甲烷的含量越多,则Z的大小为a<3<b,故B正确;
C.起始$\frac{n({H}_{2}O)}{n(C{H}_{4})}$=3,水和甲烷按1:1反应,达到平衡时,二者比值不等于3,故C错误;
D.增大压强,平衡逆向移动,所以平衡在加压后φ(CH4)增大,故D错误.
故选B.
点评 本题考查了化学平衡的影响因素及应用,为高频考点,题目难度不大,明确化学平衡及其影响为解答关键,试题侧重基础知识的考查,有利于提高学生的分析能力及灵活应用能力.


科目:高中化学 来源: 题型:填空题
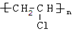 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁有剩余,溶液呈浅绿色,c(Cl-)基本不变 | |
| B. | 往溶液中滴加无色KSCN溶液,不显色 | |
| C. | 溶液中n(Fe2+)与n(Fe3+)之比为6:1 | |
| D. | 氧化产物与还原产物的物质的量之比为2:5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用试管取出试剂瓶中的Na2CO3溶液,发现取量过多,为了不浪费,又把过量的试剂倒入试剂瓶中 | |
| B. | 粗盐提纯时,为了加快过滤速率.可以用玻璃棒进行搅拌 | |
| C. | 用蒸发方法使NaCl从溶液中析出时,应将蒸发皿中NaCl溶液全部加热蒸干 | |
| D. | 用浓硫酸配制一定物质的最浓度的稀硫酸时,浓硫酸溶于水后,应冷却至室温才能转移到容量瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 以硼氢化合物NaBH4(强电解质,B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示.下列说法正确的是( )
以硼氢化合物NaBH4(强电解质,B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示.下列说法正确的是( )| A. | 电极a采用MnO2,MnO2既作电极材料又有催化作用 | |
| B. | 电池放电时Na+从b极区移向a极区 | |
| C. | 每消耗3mol H2O2,转移的电子为3mol | |
| D. | 该电池的负极反应为:BH4-+8OH--8e-═BO2-+6H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钡溶液中滴加稀硫酸:Ba2++SO42-═BaSO4↓ | |
| B. | 碳酸钙与稀硝酸反应:CO32-+2H+═CO2↑+H2O | |
| C. | 向较浓的Na2SiO3溶液中滴加适量盐酸制得硅酸胶体:SiO32-+2H+=H2SiO3(胶体) | |
| D. | 向氯化铝溶液中加过量氨水:A13++4NH3•H2O=AlO2-+2H2O+4NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钠与碳酸氢钙反应 | B. | 过氧化钠与二氧化碳反应 | ||
| C. | 单质硫与氧气反应 | D. | 铁粉与氯气反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 以上锈蚀过程是发生的化学腐蚀 | |
| B. | 从锈蚀反应的最终结果看,水既是氧化剂.又是还原剂 | |
| C. | 反应的实质是氧气被还原,金属铁被氧化 | |
| D. | 从反应机理看,锈蚀过程发生的是析氢腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2O和Na2O2组成元素相同,与CO2反应产物也相同 | |
| B. | SO2和CO2都是酸性氧化物,都能与NaOH溶液反应 | |
| C. | 工业用氢气与铁矿石在高温下反应冶炼金属铁 | |
| D. | C3H8和CH3CH2OH相对分子质量相近,分子间作用力相近,二者沸点也相近 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com