
【题目】分析下列各项结构的规律,按此规律排布第10项的分子式应为( ) 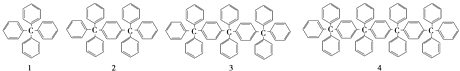
A.C198H146
B.C196H155
C.C196H146
D.C198H155
【答案】C
【解析】解:1分子式为:C25H20 , 2分子式为:C44H34 , 3分子式为:C63H48 , 由此规律得到,C的个数为25+(n﹣1)×19,H的个数为:20+(n﹣1)×15﹣(n﹣1),据此第10个分子式中C的个数为:25+(10﹣1)×19=196,H的个数为:20+(10﹣1)×15﹣(10﹣1)=146,故分子式为:C196H146 , 故选C.
【考点精析】本题主要考查了芳香烃、烃基和同系物的相关知识点,需要掌握分子里含有一个或多个苯环的碳氢化合物,称为芳香烃,其中由一个苯环和饱和烃基组成的芳香烃叫苯的同系物,其通式为CnH2n–6(n≥6)才能正确解答此题.


 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:
【题目】电化学原理在防止金属腐蚀、能量转换、物质合成等方面应用广泛. 
(1)为了减缓海水对钢闸门A和C的腐蚀,图1中,材料B可以选择(填字母序号). a.锌板 b.铜板 c.碳棒
图2中,钢闸门C作极.若用氯化钠溶液模拟海水进行实验,D为石墨块,则D上的电极
反应式为 , 检测该电极反应产物的试剂是 .
(2)微生物电池是指在微生物的作用下将化学能转化为电能的装置,其工作原理如图3所示(质子交换膜只允许H+自由通过).该电池的正极反应式为 .
(3)电渗析法处理厨房垃圾发酵液,同时得到乳酸(弱酸)的原理如图4所示(图中“HA”表示乳酸 分子,A﹣表示乳酸根离子).
①阳极的电极反应式为 .
②简述浓缩室中得到浓乳酸的原理: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在溶液中因发生氧化还原反应而不能大量共存的是
A.I-、NO3-、Fe3+、Na+B.K+、Ba2+、OH-、SO42-
C.Ag+、NO3-、Cl-、K+D.Cu2+、NH4+、Cl-、OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环己酮是一种重要的有机化工原料.实验室合成环己酮的反应如图1: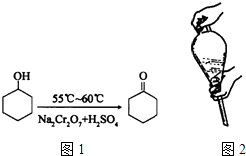
环己醇和环己酮的部分物理性质见下表:
物质 | 相对分子质量 | 沸点(℃) | 密度(gcm﹣3、20℃) | 溶解性 |
环己醇 | 100 | 161.1 | 0.9624 | 能溶于水和醚 |
环己酮 | 98 | 155.6 | 0.9478 | 微溶于水,能溶于醚 |
现以20mL环己醇与足量Na2Cr2O7和硫酸的混合液充分反应,制得主要含环己酮和水的粗产品,然后进行分离提纯.其主要步骤有(未排序):
a.蒸馏、除去乙醚后,收集151℃~156℃馏分
b.水层用乙醚(乙醚沸点34.6℃,易燃烧)萃取,萃取液并入有机层
c.过滤
d.往液体中加入NaCl固体至饱和,静置,分液
e.加入无水MgSO4固体,除去有机物中少量水
回答下列问题:
(1)上述分离提纯步骤的正确顺序是 .
(2)b中水层用乙醚萃取的目的是 .
(3)以下关于萃取分液操作的叙述中,不正确的是 .
A.水溶液中加入乙醚,转移至分液漏斗,塞上玻璃塞,如图2用力振荡
B.振荡几次后需打开分液漏斗上口的玻璃塞放气
C.经几次振荡并放气后,手持分漏斗静置液体分层
D.分液时,需先将上口玻璃塞打开或玻璃塞上的凹槽对准漏斗上的小孔,再打开旋塞,待下层液体全部流尽时,再从上口倒出上层液体
(4)在上述操作d中,加入NaCl固体的作用是 . 蒸馏除乙醚的操作中,采用的加热方式为 .
(5)蒸馏操作时,一段时间后发现未通冷凝水,应采取的正确方法是 .
(6)恢复至室温时,分离得到纯产品体积为12mL,则环己酮的产率约是(保留两位有效数字).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质俗名与化学式对应错误的是
A.胆矾 CuSO45H2O
B.重晶石 BaSO3
C.绿矾 FeSO47H2O
D.明矾KAl(SO4)212H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对某未知溶液中离子的检验方法及其结论一定正确的是( )
A.取溶液进行焰色反应显黄色,一定含有Na+
B.滴加BaCl2溶液,产生白色沉淀,证明有SO ![]()
C.滴加KSCN溶液,变为血红色,溶液中含Fe2+
D.加入稀盐酸产生无色气体,一定含有CO ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA代表阿伏加德罗常数的数值,下列说法正确的是( )
A.1mol硫酸铝钾中阴离子所带电荷总数为2NA
B.等质量的乙炔和苯分别完全燃烧,乙炔和苯都消耗7.5NA个氧气分子
C.将0.1mol碳酸钠溶于1L水中,所得溶液含有CO ![]() 和HCO
和HCO ![]() 共0.1NA个
共0.1NA个
D.在H2O2作燃料电池的负极原料时,每摩尔H2O2转移的电子数为2 NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com