
【题目】Ⅰ.向Ba(OH)2溶液中逐滴加入稀硫酸,请完成下列问题:
(1)写出反应的离子方程式__________。
(2)下列三种情况下,离子方程式与(1)相同的是____(填序号)。
A.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至溶液中显中性
B.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至SO![]() 恰好完全沉淀
恰好完全沉淀
C.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至过量
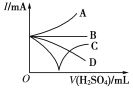
(3)若缓缓加入稀硫酸直至过量,整个过程中混合溶液的导电能力(用电流强度I表示)可近似地用右图中的___曲线表示(填序号)。
(4)若有一表面光滑的塑料小球悬浮于Ba(OH)2溶液中央,如图所示,向该烧杯里缓缓注入与Ba(OH)2溶液等密度的稀硫酸至恰好完全反应。在此实验过程中,小球将____________。
Ⅱ.某地甲、乙两厂排放污水,污水中含有下列8种离子中的4种:Ag+、Ba2+、Fe3+ 、Na+、Cl-、SO42-、NO3-、OH-(两厂所排污水不含相同离子)。两厂单独排放都会造成严重的水污染(其中甲厂的污水是碱性的),如将两厂的污水按一定比例混合,沉淀后的污水变成无色澄清的几乎只含硝酸钠的溶液而排放,污染程度会大大降低。关于两厂所排污水中所含的4种离子,你认为应该是:甲厂:________;乙厂________。
【答案】Ba2++2OH-+SO42-+2H+===BaSO4↓+2H2O A C 沉到烧杯底部 OH- Cl- SO42- Na+ Fe3+ Ba2+ Ag+ NO3—
【解析】
Ⅰ.(1)反应生成硫酸钡和水,硫酸钡和水在离子反应中均保留化学式;
(2)恰好完全反应时,溶液为中性;
(3)加入稀硫酸直至过量,恰好反应时导电性为0,过量后离子浓度增大,导电性增强;
(4)向该烧杯里缓缓注入与Ba(OH)2溶液等密度的稀硫酸至恰好完全反应,生成硫酸钡和水,溶液的密度小于Ba(OH)2溶液的密度.
Ⅱ.将两厂的污水按一定比例混合,沉淀后的污水变成无色澄清的几乎只含硝酸钠的溶液而排放,污染程度会大大降低,说明甲乙两厂的废水能反应生成沉淀,从离子能否大量共存的角度分析,甲厂呈碱性,可假设乙厂含有Ag+,则一定不含SO42-、OH-、Cl-,则SO42-、OH-、Cl-应存在与甲厂,因Ba2+与SO42-、Fe3+与OH-不能共存,则Fe3+、Ba2+存在于乙厂,根据溶液呈电中性可知,乙厂一定存在NO3-;所以乙厂含有的离子有:Ag+、Ba2+、Fe3+、NO3-,甲厂含有的离子为:Na+、Cl-、SO42-、OH-。
Ⅰ.(1)反应生成硫酸钡和水,离子反应为Ba2++2OH-+SO42-+2H+═BaSO4↓+2H2O;
(2)离子方程式(1)反应后溶液为中性,
A.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至溶液显中性,离子反应为Ba2++2OH-+SO42-+2H+═BaSO4↓+2H2O,故A选;
B.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至SO42-恰好完全沉淀,离子反应为Ba2++OH-+SO42-+H+═BaSO4↓+H2O,故B不选;
C.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至过量,离子反应为Ba2++OH-+SO42-+H+═BaSO4↓+H2O,故C不选;
故选A;
(3)加入稀硫酸直至过量,恰好反应时导电性为0,过量后离子浓度增大,导电性增强,图中只有C符合;
(4)向该烧杯里缓缓注入与Ba(OH)2溶液等密度的稀硫酸至恰好完全反应,生成硫酸钡和水,溶液的密度小于Ba(OH)2溶液的密度,塑料小球将沉到烧杯底部。
Ⅱ.将两厂的污水按一定比例混合,沉淀后的污水变成无色澄清的几乎只含硝酸钠的溶液而排放,污染程度会大大降低,说明甲乙两厂的废水能反应生成沉淀,从离子能否大量共存的角度分析,甲厂呈碱性,可假设乙厂含有Ag+,则一定不含SO42-、OH-、Cl-,则SO42-、OH-、Cl-应存在与甲厂,因Ba2+与SO42-、Fe3+与OH-不能共存,则Fe3+、Ba2+存在于乙厂,根据溶液呈电中性可知,乙厂一定存在NO3-;所以乙厂含有的离子有:Ag+、Ba2+、Fe3+、NO3-,甲厂含有的离子为:Na+、Cl-、SO42-、OH-。


科目:高中化学 来源: 题型:
【题目】一定条件下,向一带活塞的密闭容器中充入1 mol N2和3 mol H2,发生下列反应:N2(g)+3H2(g)![]() 2NH3(g),反应达到平衡后,改变下述条件,NH3平衡浓度不改变的是
2NH3(g),反应达到平衡后,改变下述条件,NH3平衡浓度不改变的是
A. 保持温度和容器压强不变,充入1 mol NH3(g)
B. 保持温度和容器体积不变,充入1 mol NH3(g)
C. 保持温度和容器压强不变,充入1 mol N2(g)
D. 保持温度和容器体积不变,充入1 mol H2(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素A、B、C、D、E、F的原子序数依次增大,A和B形成的气态化合物的水溶液呈碱性,A和D同主族,B和C相邻,F的最高价氧化物对应的水化物为无机含氧酸中的最强酸。E与B可组成化合物E3B2,且该物质遇水发生水解反应。已知利用如下图所示装置以制备E3B2,装置①用于制备B单质。

下列说法正确的是
A. E与B的简单离子的电子层结构相同,且简单离子半径B<E
B. ④⑥中依次盛装的试剂可以是NaOH溶液、碱石灰
C. D元素形成的单质与A2C不反应
D. 实验结束后,取⑤中的少量产物于试管中,加适量蒸馏水,可以产生使试管口湿润的红色石蕊试纸变蓝的气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.石油是混合物,汽油是纯净物
B.沸点:汽油>煤油>柴油
C.直馏汽油和裂化汽油成分完全相同
D.石油分馏是物理过程,石油裂化是化学过程
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1,4-环己二醇可用于生产聚酯纤维,可通过下列路线合成(某些反应的反应物和反应条件未列出):

(1)写出反应①、⑦的化学方程式:
①____________________________________________________________________________;
⑦____________________________________________________________________________。
(2)上述七个反应中属于消去反应的有____________(填反应序号)。
(3)反应⑤中可能产生一定量的副产物,其可能的结构简式为_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知723K时,2SO2(g)+O2(g)![]() 2SO3(g)△H=﹣QkJ/mol,在相同条件下,向一密闭容器中通入2mol SO2和1mol O2,达到平衡时放出的热量为Q1kJ;向另一体积相同的密闭容器中通入1mol SO2和0.5mol O2,达到平衡时放出的热量为Q2kJ。则Q1、Q2、Q满足的关系是( )
2SO3(g)△H=﹣QkJ/mol,在相同条件下,向一密闭容器中通入2mol SO2和1mol O2,达到平衡时放出的热量为Q1kJ;向另一体积相同的密闭容器中通入1mol SO2和0.5mol O2,达到平衡时放出的热量为Q2kJ。则Q1、Q2、Q满足的关系是( )
A.Q2=![]() B.Q2>
B.Q2>![]() C.Q2<Q1<Q D.Q=Q1>Q2
C.Q2<Q1<Q D.Q=Q1>Q2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将NaOH溶液分别滴加到两种一元弱酸HA和HB中,两种混合溶液的pH与离子浓度变化的关系如图所示。下列叙述正确的是

A. Ka(HA)的数量级为10-5
B. 当NaOH溶液与HB混合至中性时:c(B-)<c(HB)
C. 等浓度的NaA、NaB溶液中,水的电离程度:NaA<NaB
D. 等浓度的HB和NaA的混合溶液中:c(Na+)>c(A-)>c(B-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知SO2(g)+ 1/2 O2(g) ![]() SO3(g) △H = -98.30kJ/mol,现将4molSO2与一定量O2混合后充分反应,当放出314.56kJ热量时,SO2的转化率为_________________。
SO3(g) △H = -98.30kJ/mol,现将4molSO2与一定量O2混合后充分反应,当放出314.56kJ热量时,SO2的转化率为_________________。
(2)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)= 2Fe(s)+3CO2(g) △H= ―24.8kJ/mol
3Fe2O3(s)+ CO(g)=2Fe3O4(s)+ CO2(g) △H= ―47.2kJ/mol
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H= +640.5kJ/mol
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学反应方程式:_____________________________
(3)在一定条件下,CH4 和CO的燃烧的热化学方程式分别为:
CH4 ( g ) + 2O2 ( g ) = 2H2O ( l ) + CO2 ( g ) △H = -890 kJ/mol
2CO ( g ) + O2 ( g ) = 2CO2 ( g ) △H = -566 kJ/mol
一定量的CH4和CO的混合气体完全燃烧时,放出的热量为262.9 kJ,生成的CO2用过量的饱和石灰水完全吸收,可得到50 g白色沉淀。求混合气体中CH4 和CO的体积比_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com