
设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.1.6 g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1NA
B.0.1 mol丙烯酸中含有双键的数目为0.1NA
C.标准状况下,11.2 L苯中含有分子的数目为0.5NA
D.在过氧化钠与水的反应中,每生成0.1 mol氧气,转移电子的数目为0.4NA
科目:高中化学 来源: 题型:
下列判断正确的是( )
A.0.1 mol·L-1盐酸和0.1 mol·L-1醋酸分别与0.2 mol·L-1 NaOH溶液反应的速率相同
B.0.1 mol·L-1盐酸和0.1 mol·L-1硝酸分别与大小相同的大理石反应的速率相同
C.Al和 Fe分别与0.1 mol·L-1 硫酸反应的速率相同
Fe分别与0.1 mol·L-1 硫酸反应的速率相同
D.大理石块与大理石粉分别与0.1 mol·L-1盐酸反应的速率相同
查看答案和解析>>
科目:高中化学 来源: 题型:
作为世界卫生组织(WHO)推荐的Al级广谱、安全、高效消毒剂,二氧化氯(ClO2)在水处理领域有着广泛应用。与氯气相比,它不但具有更显著的杀菌能力,而且不会产生对人体有潜在危害的有机氯代物。
(1)反应时,ClO2生成ClO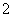 、Cl-的转化率与溶液的pH的关系如图所示。则pH=8时,ClO2被还原为________。
、Cl-的转化率与溶液的pH的关系如图所示。则pH=8时,ClO2被还原为________。
2亚氯酸根离子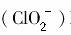 对人体不利。欲在弱碱性条件下将水中的
对人体不利。欲在弱碱性条件下将水中的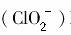 转化为Cl-除去,若该反应体系中的物质有:NaClO2、FeOH3、NaHCO3、FeCl2、NaCl、H2O、CO2。写出并配平有关化学方程式,并标出电子转移的方向和数目。
转化为Cl-除去,若该反应体系中的物质有:NaClO2、FeOH3、NaHCO3、FeCl2、NaCl、H2O、CO2。写出并配平有关化学方程式,并标出电子转移的方向和数目。

查看答案和解析>>
科目:高中化学 来源: 题型:
能在无色水溶液中大量共存的一组离子是( )
A.H+、Fe3+、I-、Cl-
B.Al3+、Mg2+、NO 、Cl-
、Cl-
C.K+、Ag+、Ca2+、CO
D.NH 、Na+、AlO
、Na+、AlO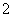 、MnO
、MnO
查看答案和解析>>
科目:高中化学 来源: 题型:
下列解释事实的方程式不准确的是( )
A.用浓盐酸检验氨:NH3+HCl===NH4Cl
B.碳酸钠溶液显碱性:CO +H2OHCO
+H2OHCO +OH-
+OH-
C.钢铁发生吸氧腐蚀时,铁作负极被氧化:Fe-3e-===Fe3+
D.长期盛放石灰水的试剂瓶内壁出现白色固体:Ca(OH)2+CO2===CaCO3↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的数值,下列说法中正确的是( )
A.标准状况下,22.4 L CCl4中含有的CCl4分子数为NA
B.1.0 L 0.1 mol·L-1的Na2S溶液中含有的S2-的数目为0.1NA
C.在密闭容器中充入1.5 mol H2和0.5 mol N2,充分反应后可得到NH3的分子数为NA
D.1 mol Fe与过量的稀HNO3反应,转移3NA个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
NA表示阿伏加德罗常数的值,下列说法中正确的是(双选)( )
A.100 mL 1 mol·L-1 Na2CO3溶液中溶质离子的总数小于0.3NA
B.若120 g的墨粉(只含碳)能打a个字,则平均每个字约含有10NA/a个碳原子
C.25℃、101 kPa时,0.1NA个H2分子完全燃烧生成液态水,放出a kJ热量,表示氢气燃烧热的热化学方程式为H2(g)+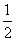 O2(g)===H2O(l) ΔH=+10a kJ·mol-1
O2(g)===H2O(l) ΔH=+10a kJ·mol-1
D.常温下28 g 14CO中含有14NA个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
根据下列实验内容得出的结论正确的是( )
| 选项 | 实验内容 | 结论 |
| A | 某物质的水溶液使红色石蕊试纸变蓝 | 该物质一定是碱 |
| B | 某气体能使湿润的淀粉碘化钾试纸变蓝 | 该气体一定是氯气 |
| C | 向某物质的水溶液中加入盐酸,产生无色无味气体 | 该溶液中一定含有碳酸根离子 |
| D | 向铁和稀硝酸反应后的溶液中滴入KSCN溶液,溶液显血红色 | 反应后溶液中肯定有Fe3+,可能还有Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度时,在一个容积为2 L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:
(1)该反应的化学方程式为____________________________________。
(2)反应开始至2 min,气体Z的反应速率为_____________________。
(3)若X、Y、Z均为气体,反应达到平衡时:
①压强是开始时的________倍;
 ②若此时将容器的体积缩小为原来的
②若此时将容器的体积缩小为原来的 倍,达到平衡时,容器内温度将升高(容器不与外界进行热交换),则该反应的正反应为________反应(填“放热”或“吸热”)。
倍,达到平衡时,容器内温度将升高(容器不与外界进行热交换),则该反应的正反应为________反应(填“放热”或“吸热”)。
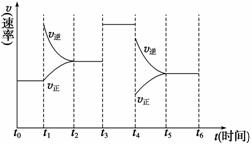
(4)若上述反应在2 min后的t1~t6内反应速率与反应时间图像如右,在每一时刻均改变一个影响反应速率的因素,则( )
A.在t1时增大了压强 B.在t3时加入了催化剂
C.在t4时降低了温度 D.t2~t3时X的转化率最高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com