(2011?延庆县一模)海水蕴含着丰富的资源.在化学实验室里模拟从海水中提取重要的工业原料氯化钠时,设计了以下操作流程:
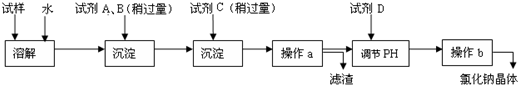
请回答以下问题:
(1)在所提供的试剂中选择:试剂C是
①
①
①Na
2CO
3 ②BaCl
2 ③稀盐酸
(2)操作b中用到的主要仪器为酒精灯、
蒸发皿
蒸发皿
、三脚架和玻璃棒.
(3)利用所得的氯化钠制氯气和氢气,并检验氯气的氧化性和测定产生氢气的体积.试按如图所给仪器,设计一套能完成以上实验目的装置,仪器接口的正确连接顺序是:
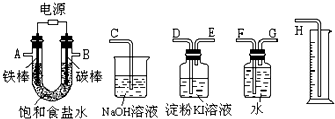
A接
G
G
,
F
F
接
H
H
;B接
D
D
,
E
E
接
C
C
.
(4)写出通入C后,烧杯中所发生的离子反应方程式
Cl2+2OH-═Cl-+ClO-+H2O;
Cl2+2OH-═Cl-+ClO-+H2O;
(5)电解氯化钠溶液时的离子方程式为
若装入的饱和食盐水为75mL,接通电源一段时间,停止通电后,测得氢气为8.4mL(标准状况).将U形管内的溶液混合均匀,其
pH约为
12
12
.(假设电解前后溶液体积变化可忽略不计,产生的气体全部逸出)
(6)若想准确读取所得氢气的体积,应采取的操作有
量筒中液面和广口瓶液面相平;读数时视线与量筒凹液面相平;待整套装置恢复至室温时再行读取数据,
量筒中液面和广口瓶液面相平;读数时视线与量筒凹液面相平;待整套装置恢复至室温时再行读取数据,
.




