
 ;A与C组成的化合物为MgS(用具体元素符号表示).
;A与C组成的化合物为MgS(用具体元素符号表示).分析 A、B、C是三种元素的原子,质子数都小于18,A原子与B原子的最外层电子数都是6,A、B都属于第VIA族元素,A原子与C原子的核外电子层数都为3,则A、C都是第三周期元素,则A位于第三周期第VIA族,则A是S元素,B为O元素,C原子的质子数比A少4,则C是Mg元素,
(1)通过以上分析确定这元素种类;
(2)A离子核外有3个电子层、最外层电子数是8,据此确定A离子结构示意图;A、C元素通过得失电子形成离子化合物硫化镁;
(3)元素A的一种质量数为32的核素,与元素B的一种核素构成微粒为AB42-,1molSO42-的质量为104g,则硫酸根离子的摩尔质量是104g/mol,摩尔质量在数值上等于其相对分子质量,所以该硫酸根离子相对分子质量为104,先计算每个氧原子相对原子质量,一种核素的相对原子质量在数值上等于质子数+中子数,据此计算元素B的该核素中的中子数.
解答 解:A、B、C是三种元素的原子,质子数都小于18,A原子与B原子的最外层电子数都是6,A、B都属于第VIA族元素,A原子与C原子的核外电子层数都为3,则A、C都是第三周期元素,则A位于第三周期第VIA族,则A是S元素,B为O元素,C原子的质子数比A少4,则C是Mg元素,
(1)通过以上分析知,A、B分别是S、O元素,
故答案为:S;O;
(2)A离子核外有3个电子层、最外层电子数是8,则A离子结构示意图为 ;A、C元素通过得失电子形成离子化合物MgS,
;A、C元素通过得失电子形成离子化合物MgS,
故答案为: ;MgS;
;MgS;
(3)1molSO42-的质量为104g,则硫酸根离子的摩尔质量是104g/mol,摩尔质量在数值上等于其相对分子质量,所以该硫酸根离子相对分子质量为104,该氧原子相对原子质量=$\frac{104-32}{4}$=18,核素的相对原子质量在数值上等于其质量数,该氧原子质子数是8,则中子数=18-8=10,
故答案为:10.
点评 本题考查位置结构性质的相互关系及应用,熟练原子结构、元素周期表结构、物质结构是解本题关键,知道元素化合物的性质,注意元素元素相对原子质量与该元素的一种原子相对原子质量的关系,为易错点,题目难度中等.


 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:高中化学 来源: 题型:解答题
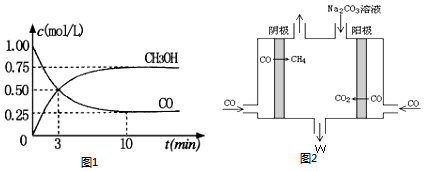
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水电离出的c(H+)=10-13mol•L溶液:Na+、NH4+、CO32-、SO42- | |
| B. | 澄清透明溶液:Mg2+、Cu2+、SO42-、Cl- | |
| C. | 0.1mol•L-1FeCl3溶液:K+、NH4+、I-、SCN- | |
| D. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=1×1014溶液:Ba2+、Na+、ClO-、NO- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 时间/s | 0 | 20 | 40 | 60 | 80 | 100 |
| c(NO2)/mol•L-1 | 0.00 | 0.12 | 0.20 | 0.26 | 0.30 | 0.30 |
| A. | 20~40s内,v(N2O4)=0.004mol/(L•s) | |
| B. | 在相同条件下,开始时若向容器中充入的是0.80 molNO2,达到平衡后NO2的转化率为75% | |
| C. | 反应达平衡时,吸收的热量为15.9 kJ | |
| D. | 100 s时再通入0.40 mol N2O4,达新平衡时N2O4的转化率增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
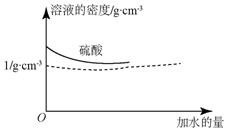 已知硫酸的密度与所加水量的关系如图所示,
已知硫酸的密度与所加水量的关系如图所示,查看答案和解析>>
科目:高中化学 来源: 题型:推断题
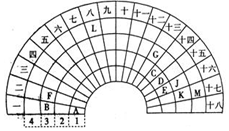 元素周期表的形式多种多样,如图是扇形元素周期表的一部分(前四周期的元素),对比中学常见元素周期表,回答下列问题:
元素周期表的形式多种多样,如图是扇形元素周期表的一部分(前四周期的元素),对比中学常见元素周期表,回答下列问题: .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④ | B. | ②③④ | C. | ② | D. | ②⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
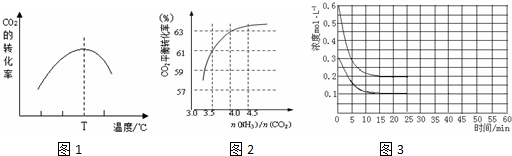
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com