
下图中A、B、C、D分别代表有关反应中的一种化合物,其中物质A是一种高熔点化合物,
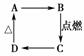
不溶于硫酸、硝酸,却溶于氢氟酸。请填写以下空白。
(1)A、B、C、D的化学式分别是________、________、________、________。
(2)A→B的化学方程式是____________________________________________。
(3)C→D的离子方程式是_____________________________________________。
 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案科目:高中化学 来源: 题型:
等物质的量的CO和CO2相比较,下列有关叙述中正确的是( )
①它们所含的分子数之比为1∶1 ②它们所含的O原子数目之比为1∶2 ③它们所含的原子总数目之比为2∶3 ④它们所含的C原子数目之比为1∶1 ⑤它们所含的电子数目之比为7∶11
A.①和④ B.②和③
C.④和⑤ D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学兴趣小组测定某FeCl3样品(只含少量FeCl2杂质)中铁元素的质量分数,按以下实验步骤进行操作:
① 称取a g样品,置于烧杯中;
② 加入适量盐酸和蒸馏水,使样品溶解,然后准确配制成250.00mL溶液;
③ 量取25.00mL步骤②中配得的溶液,置于烧杯中,加入适量的氯水,使反应完全;
④ 加入过量氨水,充分搅拌,使沉淀完全;
⑤ 过滤,洗涤沉淀;
⑥ 将沉淀转移到某容器内,加热、搅拌,直到固体由红褐色全部变为红棕色后,在干燥器中冷却至室温后,称量;
⑦……。
请根据上面叙述,回答:
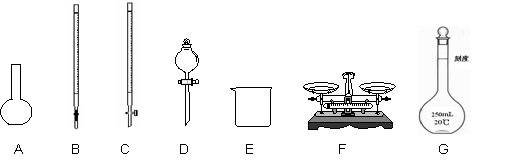
(1)上图所示仪器中,本实验步骤①②③中必须用到的仪器是E,F和 (填字母)。
(2)步骤②中加入盐酸的作用____________________________ ______。
(3)写出步骤④中发生反应的离子方程式 。
(4)样品中的杂质Fe2+有较强的还原性,完成并配平下列反应的离子方程式
___Fe2+ + ___ClO3— + = __Fe3+ + ___Cl— + ___H2O
从理论上分析,上述实验中若将氯水改为NaClO3时,对实验结果造成 (填偏大、偏小或不影响).
(5)第⑥步的操作中,将沉淀物转移到 (填仪器名称)中加热,冷却至室温,称量其质量为m1g.
(6)本实验若容器质量是W1 g,最终容器和固体的总质量是W2 g,则样品中铁元素的质量分数为 。(列出算式,不需化简)
(7)已知Cl2与热的NaOH溶液可发生如下反应:
3Cl2 + 6NaOH  5NaCl + NaClO3 + 3H2O
5NaCl + NaClO3 + 3H2O
则Fe3+、KClO3、Cl2三种物质其氧化性在酸性溶液由强到弱的顺序是_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中,正确的是( )
A.制造水泥和普通玻璃的原料中都含有石灰石
B.普通玻璃是电的绝缘体,这种透明的固体物质熔点很低
C.石英玻璃能经受温度剧变且能抵抗酸碱的腐蚀
D.硅酸盐可用氧化物形式表示其组成,这表明硅酸盐是由氧化物组成的
查看答案和解析>>
科目:高中化学 来源: 题型:
将等物质的量的镁和铝相混合,平均分成4份,分别加到足量的下列溶液中,充分反应后,放出氢气最多的是( )
A.3 mol·L-1HCl B.4 mol·L-1HNO3
C.8 mol·L-1NaOH D.18 mol·L-1H2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
在电子工业中,制印刷电路时,常用氯化铁溶液作为铜的腐蚀液,该过程发生的反应为2FeCl3+Cu===2FeCl2+CuCl2。该反应利用了铜的什么性质( )
A.氧化性 B.还原性
C.导电性 D.导热性
查看答案和解析>>
科目:高中化学 来源: 题型:
下图标出了各种材料强度与密度的比值以及广泛使用的年代。
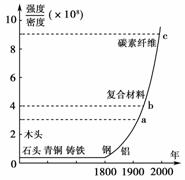
有甲、乙两种材料,它们的强度相同,甲的密度是乙的2倍。且甲材料在图中与b点对应,则乙材料在图中的位置是( )
A.a点 B.a、b之间
C.c点 D.b、c之间
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com