
【题目】下图表示的一些物质或概念间的从属关系中正确的是

X | Y | Z | |
A | 二氧化氮 | 酸性氧化物 | 氧化物 |
B | 硫酸 | 化合物 | 电解质 |
C | 胶体 | 分散系 | 混合物 |
D | 置换反应 | 氧化还原反应 | 离子反应 |
A. A B. B C. C D. D
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案科目:高中化学 来源: 题型:
【题目】国家卫健委公布的新型冠状病毒肺炎诊疗方案指出,乙醚、75%乙醇、含氯消毒剂、过氧乙酸(CH3COOOH)、氯仿等均可有效灭活病毒。对于上述化学药品,下列说法错误的是
A.CH3CH2OH能与水互溶
B.NaClO通过氧化灭活病毒
C.过氧乙酸相对分子质量为76
D.氯仿的化学名称是四氯化碳
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对 于2NO2(g)![]() N2O4(g) 的反应体系,在压强一定时,平衡体系中N2O4的质量分数w(N2O4) 随温度的变化情况如图所示(实线上的任何一点为对应温度下的平衡状态)。
N2O4(g) 的反应体系,在压强一定时,平衡体系中N2O4的质量分数w(N2O4) 随温度的变化情况如图所示(实线上的任何一点为对应温度下的平衡状态)。

(1)该反应的正反应方向是一个______反应(填“吸热”或“放热”)。
(2)A、B、C、D、E 各状态中,v(正)逆)的是_________。
(3)维持t1不变,E→A所需时间为x, 维持t2不变,D→C所需时间为y.则x_____y(填“<”、“>”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一支25mL酸式滴定管中盛盐酸,液面恰好在amL刻度处,把管内液体全部放出,盛入量筒内,所得液体体积一定是( )
A.a mL
B.(25﹣a)mL
C.大于(25﹣a)mL
D.大于a mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作正确的是
A.用酒精萃取碘水中的碘
B.用蒸馏的方法制取蒸馏水
C.用过滤的方法除去食盐水中的硫酸钠
D.分液时,分液漏斗中的液体全部从下口放出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaC1O2是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下: 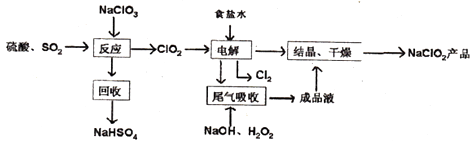
回答下列问题:
(1)“电解”所用食盐水由粗盐水精制而成,精制对,为除去Mg2+和Ca2+ , 要加入的试剂分别为、 .
(2)写出“反应”步骤中生成ClO2的化学方程式 .
(3)实验所用原料硫酸是由浓硫酸稀释而获得,写出实验过程 .
(4)“尾气吸收”是吸收“电解”过程排出的少量ClO2 . 此吸收反应中,氧化剂与还原剂的物质的量之比为 .
(5)将lmolSO2和lmolC12通入水中形成lL的溶液,所得溶液中氢离子浓度为mol/L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于生活中的有机物,下列说法正确的是( )
A. 所有的糖类、油脂和蛋白质都能发生水解反应
B. 工业上利用油脂在碱性条件下的水解反应制取肥皂和甘油
C. 做衣服的棉、麻、蚕丝的主要成分都是纤维素
D. 人体中没有水解纤维素的酶,所以纤维素在人体中没有任何作用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】今年6月20日,2016年全球最受关注的十大化学成果发布,其中有两项与空气中的二氧化碳处理利用技术有关。其一为美国伊利诺斯大学芝加哥分校和阿贡国家实验室科学家联合设计的新型太阳能电池,可直接把大气中的二氧化碳转化为合成气(CO和H2)该设计同时具有环保和经济价值,不仅可以减缓二氧化碳的排放,而且可以生成重要的化工原料。
(1)下列材料也可以用于制造太阳能电池的是____________。
A.Ag2O B.Fe3O4 C.Si D.SiO2
(2)下图装置可实现二氧化碳到一氧化碳的转化

①电源的正极为______(“A”或“B")。
②阴极发生反应的电极方程式为:___________.
(3)CO 和H2可用于合成甲醇。
①已知CO、H2、CH3OH(1)的燃烧热为283.0kJ/mol、285. 8kJ/mol、726.5kJ/mol,写出 由CO和H2制备CH3OH(1)的热化学方程式__________。
②在398K,1L的恒容容器中充入0.1molCO和0.2molH2,发生反应CO(g)+2H2(g)=CH3OH(g),反应过程中气体的压强如下表所示(atm为标准大气压)。
时间(min) | 0 | 1 | 5 | 10 | 30 | 50 |
压强(atm) | 10 | 9.3 | 8.0 | 7.2 | 4 | 4 |
5min内该反应的平均速率用CO可表示为______,该温度下的平衡常数是_____。达到平衡后,向该容器中通入0.05mol的气态CH3OH,再次达到平衡时,CH3OH的体积分数比原平衡时_____( 填“大”或“小”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的性质与用途具有对应关系的是
A.铝的金属活泼性强,可用于制作铝金属制品
B.氧化铝熔点高,可用作电解冶炼铝的原料
C.氢氧化铝受热分解,可用于中和过多的胃酸
D.明矾溶于水并水解形成胶体,可用于净水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com