
| A. | 因SiO2不溶于水,故H2SiO3不是SiO2对应的酸或者SiO2不是H2SiO3的酸酐 | |
| B. | CO2通入水玻璃,可以得到硅酸沉淀 | |
| C. | SiO2是一种空间立体网状结构的晶体,熔点高,硬度大 | |
| D. | 氢氟酸能够腐蚀玻璃,故不能用玻璃瓶来装氢氟酸 |
分析 A.二氧化硅不溶于水,但二氧化硅是硅酸的酸酐;
B.碳酸酸性强于硅酸,通入水玻璃中得到硅酸沉淀;
C.二氧化硅中每个硅原子周围连有四个氧原子,每个氧原子周围连有2个硅原子,形成原子晶体;
D.氢氟酸(HF)对玻璃有腐蚀作用,故不能用玻璃瓶来盛放氢氟酸.
解答 解:A.含氧酸的分子中,氢、氧原子以水分子的组成比失去后,形成的氧化物叫做该酸的酸酐,所以硅酸(H2SiO3)的酸酐是二氧化硅(SiO2),故A错误;
B.根据强酸制弱酸,二氧化碳通入水玻璃中发生Na2SiO3+H2O+CO2=Na2CO3+H2SiO3↓,故B正确;
C.二氧化硅晶体中Si与O以共价键结合,每个Si原子能形成4个共价键,即每个Si原子结合4个O原子,并向空间伸展成网状结构是属于原子晶体,原子晶体熔点高,硬度大,故C正确;
D.氢氟酸能和玻璃成分二氧化硅反应4HF+SiO2═SiF4↑+2H2O,能够雕刻玻璃,故不能用玻璃瓶来盛放氢氟酸,故D正确;
故选A.
点评 本题主要考查硅及其化合物的性质与应用,注意二氧化硅的晶体类型及性质,侧重于基础知识的考查,题目难度不大.


 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:高中化学 来源: 题型:选择题
| A. | ①②③⑤ | B. | ②③⑤ | C. | ③④⑤ | D. | ①③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCl(H2S) | B. | O2(N2) | C. | CO(H2S) | D. | H2S(HCl) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba(OH)2、Na2S03、FeCl3、KCl | B. | Na2Si03、Na2C03、KN03、NH4Cl | ||
| C. | NH3、H20、H3P04、Na2S04、H2S04 | D. | HCl、CH2COOH、C2H5OH、Na2SiO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度(K)CO2 转化率(%) n(H2)/n(CO2) | 500 | 600 | 700 | 800 |
| 1.5 | 45 | 33 | 20 | 12 |
| 2 | 60 | 43 | 28 | 15 |
| 3 | 83 | 62 | 37 | 22 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+ Na+ NO3- CO32- | B. | Na十 Fe3+ SCN- SO42- | ||
| C. | K+ Na十 Cl- AlO2- | D. | Al3+ Na+ Cl- SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:填空题
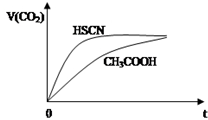 已知25℃时有关弱酸的电离平衡常数:
已知25℃时有关弱酸的电离平衡常数:| 弱酸化学式 | HSCN | CH3COOH | HCN | H2CO3 |
| 电离平衡常数 | 1.3×10-1 | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠质软,可用小刀切割 | |
| B. | 钠要保存在煤油或者石蜡油中 | |
| C. | 钠着火可用干沙扑灭 | |
| D. | 钠与氧气反应,产物是由氧气的量决定的 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com