
����Ŀ��ij�ᾧˮ���ﺬ�����������Ӻ�һ�������ӣ���ȡ����������Ϊ1.96g�ĸýᾧˮ����ֱ��Ƴ���Һ�� һ�ݼ�������Ba��OH��2��Һ�����ɰ�ɫ�������漴������Ϊ����ɫ�������к��ɫ�����ȸû����ݳ�0.224L����״������ʹʪ��ĺ�ɫʯ����ֽ���������壻��ϡ���ᴦ���������ϴ�Ӻ���õ���ɫ����2.33g��
��һ�ݼ��뺬0.001molKMnO4��������Һ��MnO4��ǡ����ȫ����ԭΪMn2+ ��
��ش��������⣺
��1���ýᾧˮ�����к��е��������������� �� �������� ��
��2���ýᾧˮ����Ļ�ѧʽ ��
���𰸡�
��1��NH4+��Fe2+��SO42��
��2����NH4��2Fe��SO4��2?6H2O��[��NH4��2SO4?FeSO4?6H2O]
���������⣺��1��һ�ݼ�������Ba��OH��2��Һ�����ɰ�ɫ�������漴������Ϊ����ɫ�������к��ɫ��˵������Fe2+���ӣ����ȸû����ݳ�0.224L����״������ʹʪ��ĺ�ɫʯ����ֽ���������壬˵������NH4+ �� ��ϡ���ᴦ���������ϴ�Ӻ���õ���ɫ����2.33g��˵������SO42�� �� ���Դ��ǣ�NH4+��Fe2+��SO42������2����������Ϣ��֪1.96g�ĸýᾧˮ�����У�n��NH4+��= ![]() =0.01mol������Ϊ��m��NH4+��=0.01mol��18g/mol=0.18g��n��SO42����=
=0.01mol������Ϊ��m��NH4+��=0.01mol��18g/mol=0.18g��n��SO42����= ![]() =0.01mol������Ϊ��m��SO42����=0.01mol��96g/mol=0.96g��KMnO4��������Һ���������ԣ���Fe2+����������ԭ��Ӧ�����ݵ�ʧ���ӵ����ʵ�����ȣ� ���У�0.001mol����7��2��=n����3��2��n=0.005mol����Fe2+�����ʵ���Ϊ0.005mol������Ϊ��0.005mol��56g/mol=0.28g�����Խᾧˮ������ˮ������Ϊ��1.96g��0.18g��0.96g��0.28g=0.54g��n��H2O��=
=0.01mol������Ϊ��m��SO42����=0.01mol��96g/mol=0.96g��KMnO4��������Һ���������ԣ���Fe2+����������ԭ��Ӧ�����ݵ�ʧ���ӵ����ʵ�����ȣ� ���У�0.001mol����7��2��=n����3��2��n=0.005mol����Fe2+�����ʵ���Ϊ0.005mol������Ϊ��0.005mol��56g/mol=0.28g�����Խᾧˮ������ˮ������Ϊ��1.96g��0.18g��0.96g��0.28g=0.54g��n��H2O��= ![]() =0.03mol�����ԣ�1.96g�ĸýᾧˮ�����У�m��NH4+����n��Fe2+����n��SO42������n��H2O��=0.01mol��0.005mol��0.01mol��0.03mol=2��1��2��6���ýᾧˮ����Ļ�ѧʽΪ����NH4��2Fe��SO4��26H2O��[��NH4��2SO4FeSO46H2O]�����Դ��ǣ���NH4��2Fe��SO4��26H2O��[��NH4��2SO4FeSO46H2O]��
=0.03mol�����ԣ�1.96g�ĸýᾧˮ�����У�m��NH4+����n��Fe2+����n��SO42������n��H2O��=0.01mol��0.005mol��0.01mol��0.03mol=2��1��2��6���ýᾧˮ����Ļ�ѧʽΪ����NH4��2Fe��SO4��26H2O��[��NH4��2SO4FeSO46H2O]�����Դ��ǣ���NH4��2Fe��SO4��26H2O��[��NH4��2SO4FeSO46H2O]��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͬѧͨ����ѯ����֪����һ��Ũ�ȵ�������Mg��Ӧʱ����ͬʱ�õ�NO2��NO��N2�������塣��ͬѧ��������������װװ����ֱ����֤��NO2��NO���ɲ���ȡ����þ (����ʵ����ÿ��ת��������ȫ��) ����������֪��
��NO2�е�Ϊ21.1 �桢�۵�Ϊ��11 �棬NO�е�Ϊ��151 �桢�۵�Ϊ��164 �棻
��þҲ����CO2��Ӧ��
�۵���þ��ˮ����ˮ������Mg(OH)2�Ͱ�����

��1��Ϊʵ������ʵ��Ŀ�ģ���ѡ�õ���������ȷ���ӷ�ʽ�ǣ�A�� ��E��ʵ�����ȴ���K��ͨ��������װ����ͨ��CO2�������ų�װ���ڵĿ�����ֹͣͨ��CO2�ı�־�� ��
��2��ȷ����ԭ��������NO2�������� ��ʵ����Ҫ���ʹ��װ��F���ڶ���ʹ��F��Ŀ���� ��
��3��ʵ������У�������D�в���Ԥ�������ͬʱ��C����Һ��ɫ������ȥ����д��C�з�Ӧ�����ӷ���ʽ ��
��4����ͬѧ��A�п�ʼ��Ӧʱ�����ϵ�ȼB���ľƾ��ƣ�ʵ�������ͨ�����Է���B���IJ�Ʒ���Ȳ��ߣ�ԭ���� ��
��5�����һ��ʵ�鷽������֤þ�����ᷴӦʱȷʵ�а������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͭ��CuFeS2������ȡͭ���仯�������Ҫԭ��֮һ���������Ʊ������Ļ����
��1��ұ��ͭ�ķ�ӦΪ8CuFeS2+21O2 ![]() 8Cu+4FeO+2Fe2O3+16SO2��CuFeS2��Fe�Ļ��ϼ�Ϊ+2����Ӧ�б���ԭ��Ԫ��������Ԫ�ط��ţ���
8Cu+4FeO+2Fe2O3+16SO2��CuFeS2��Fe�Ļ��ϼ�Ϊ+2����Ӧ�б���ԭ��Ԫ��������Ԫ�ط��ţ���
��2��ұ��ͭ����Ҫ������ͼ1�� 
������A�еĴ�����Ⱦ���ѡ�������Լ��е����գ�
a��ŨH2SO4 b��ϡHNO3 c��NaOH��Һ
����ϡHNO3��������B��ȡ����������Һ���μ�KSCN��Һ��ʺ�ɫ��һλͬѧ�ɴ˵ó�����������Ԫ�ؼ�̬Ϊ+3�Ľ��ۣ���ָ���ý����Ƿ������˵������
��3��ұ������ͭ���Է������з�Ӧ��ͼ2�� ��д��Cu����ϡH2SO4��H2O2���Һ�����ӷ���ʽ�� ��
��д��Cl2��Z����ΪK2EO4�Ļ�ѧ����ʽ�� ��
�۶���0.1molL��1 CuSO4��Һ����ȷ���� ��
A�������£�pH��7
B��c��Cu2+����c��SO42������c��H+����c��OH����
C��c��H+��+2c��Cu2+��=2c��SO42����+c��OH����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2015��9��1�գ��Ĵ�������˸�����ӭ��118�����ա��п�ѧ�Ҷ������������м��������ĸ��״�л����������Ҷ�������������dz��ã��������ۣ�����Ѫ�ܼ����ļ���Ҳ�ܵͣ�����һ����й��ˣ�֬�ʴ�л���������縶���塣���ϲ��ϻش��������⣺
��1��֬����ϸ������Ҫ�Ļ�������У� �������֬�ʣ�Ҳ��ϸ�������õĴ������ʣ�����֮�⣬������ �� ��___________�Ĺ��ܡ������е� �ǹ���ϸ��Ĥ����Ҫ�ɷ֡�
��2����ʳ�й�������� ������Ѫ�ܱ����γɳ��������Ѫ�ܶ�����
��3��֬������ǡ������ʡ����ᶼ��ϸ������Ҫ���л���������к��������������ӣ����������� Ϊ�Ǽܣ����Ƕ����������������ɵ�λ���Ӷ��ɣ���Щ�����ĵ�λ��Ϊ���塣
��4����ɵ����ʵĵ���ķ��ӽṹͨʽ�ǣ� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������þ�㷺������ȼ��������������ʯ����ѧʽ��MgCO3CaCO3��Ϊԭ���Ʊ�������þ�Ĺ����������£� 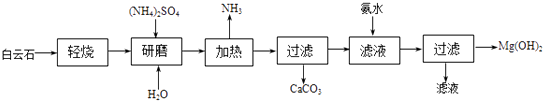
��1����������ͼ������ʯ�����ա��ֽ�Ļ�ѧ��Ӧʽ�� ��
��2������ĥ����Ŀ���� ��
��3�����백ˮʱ��Ӧ�Ļ�ѧ����ʽΪ������Mg��OH��2�����Ƿ�ϴ�Ӹɾ��ķ����� ��
��4���������п���ѭ�����õ������� ��
��5����ͳ�����ǽ�����ʯ���·ֽ�Ϊ����þ�������ƺ���ȡ�����ù��ղ������հ���ʯ�ķ��������ŵ��� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����в�Ʒ����Ҫ�ɷֲ���ȷ����( )
A.���������
B.ˮ������������
C.Ư������������ƺ��Ȼ���
D.�մ�����̼����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����( )
A.�õ��۵⻯����ֽ�����ˮ����ˮ
B.�������������Ư��ֽ��
C.þ�Ż�ʱ���ö�����̼��������
D.������ͭ�������������ϸ������ͭת��Ϊͭ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʵ��Ʊ��������Ϲ�ҵ����ʵ�ʵ��ǣ� ��
A.��������Ȼ�þ�Ƶ���þ
B.�����̿��Ũ�����ڼ���������������
C.�ö��������ڸ������뽹̿��Ӧ�Ƶôֹ�
D.��ҵ������ʱ������ʯ��ʯ��ȥ����ʯ�е�SiO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ��R��T��Q��W��Ԫ�����ڱ��е����λ����ͼ��ʾ������T������������������������ȣ������жϲ���ȷ���ǣ� �� 
A.�����̬�⻯������ȶ��ԣ�R��Q
B.����������Ӧˮ��������ԣ�Q��W
C.ԭ�Ӱ뾶��T��Q��R
D.T������������Ӧ��ˮ���ﲻ�ܺ�ǿ�Ӧ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com