
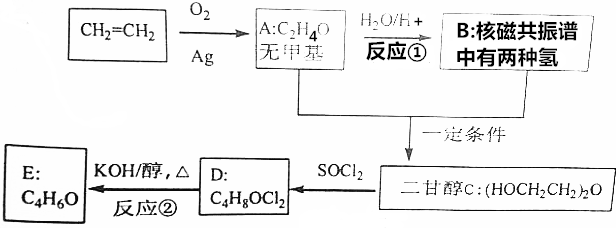
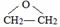 DClCH2CH2OCH2CH2Cl;
DClCH2CH2OCH2CH2Cl;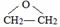 +H2O$\stackrel{H+}{→}$HOCH2CH2OH;反应②ClCH2CH2OCH2CH2Cl+2KOH$→_{△}^{醇}$CH2=CHOCH=CH2+2KCl+2H2O;
+H2O$\stackrel{H+}{→}$HOCH2CH2OH;反应②ClCH2CH2OCH2CH2Cl+2KOH$→_{△}^{醇}$CH2=CHOCH=CH2+2KCl+2H2O;分析 乙烯发生氧化反应生成A(C2H4O),A的结构中没有甲基,则A为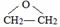 ,A在酸性条件下水解得到B,B的核磁共振氢谱有2种H,结合二甘醇的结构可知B为HOCH2CH2OH.二甘醇发生信息中的反应得到D,结合D的分子式可知D的结构简式为ClCH2CH2OCH2CH2Cl,D发生消去反应生成E为CH2=CHOCH=CH2.
,A在酸性条件下水解得到B,B的核磁共振氢谱有2种H,结合二甘醇的结构可知B为HOCH2CH2OH.二甘醇发生信息中的反应得到D,结合D的分子式可知D的结构简式为ClCH2CH2OCH2CH2Cl,D发生消去反应生成E为CH2=CHOCH=CH2.
解答 解:乙烯发生氧化反应生成A(C2H4O),A的结构中没有甲基,则A为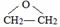 ,A在酸性条件下水解得到B,B的核磁共振氢谱有2种H,结合二甘醇的结构可知B为HOCH2CH2OH.二甘醇发生信息中的反应得到D,结合D的分子式可知D的结构简式为ClCH2CH2OCH2CH2Cl,D发生消去反应生成E为CH2=CHOCH=CH2.
,A在酸性条件下水解得到B,B的核磁共振氢谱有2种H,结合二甘醇的结构可知B为HOCH2CH2OH.二甘醇发生信息中的反应得到D,结合D的分子式可知D的结构简式为ClCH2CH2OCH2CH2Cl,D发生消去反应生成E为CH2=CHOCH=CH2.
(1)由上述分析可知,A的结构简式为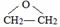 ,D的结构简式为:ClCH2CH2OCH2CH2Cl,
,D的结构简式为:ClCH2CH2OCH2CH2Cl,
故答案为: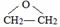 ;ClCH2CH2OCH2CH2Cl;
;ClCH2CH2OCH2CH2Cl;
(2)反应①属于水解反应,反应②属于消去反应,
故答案为:水解反应;消去反应;
(3)反应①的化学方程式为: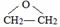 +H2O$\stackrel{H+}{→}$HOCH2CH2OH,
+H2O$\stackrel{H+}{→}$HOCH2CH2OH,
反应②的化学方程式为:ClCH2CH2OCH2CH2Cl+2KOH$→_{△}^{醇}$CH2=CHOCH=CH2+2KCl+2H2O,
故答案为: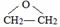 +H2O$\stackrel{H+}{→}$HOCH2CH2OH;ClCH2CH2OCH2CH2Cl+2KOH$→_{△}^{醇}$CH2=CHOCH=CH2+2KCl+2H2O;
+H2O$\stackrel{H+}{→}$HOCH2CH2OH;ClCH2CH2OCH2CH2Cl+2KOH$→_{△}^{醇}$CH2=CHOCH=CH2+2KCl+2H2O;
(4)a.含有2个羟基,与水形成氢键,应易溶于水,故a错误;
b.分子之间形成氢键,沸点较高,故b正确;
c.属于烃的含氧衍生物,能燃烧,故c错误;
d.含有羟基,可与金属钠反应,故d正确,
故选:bd.
点评 本题考查有机物的推断与合成,涉及有机反应类型、有机反应方程式书写、有机物的结构与性质等,侧重考查学生分析推理能力,熟练掌握官能团的性质与转化.


 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | X、Y、Z的热稳定性逐渐增强 | |
| B. | A、B、C、D只能形成5种单质 | |
| C. | A、B的氧化物的水化物的酸性逐渐增强 | |
| D. | 由B、C、D三种元素组成的化合物中只能形成共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 Li2CO3+Li2SiO3;该反应为放(填“吸”或者“放”)热反应,原因是升高温度,平衡向逆向进行,说明逆反应为吸热反应,所以正反应为放热反应.
Li2CO3+Li2SiO3;该反应为放(填“吸”或者“放”)热反应,原因是升高温度,平衡向逆向进行,说明逆反应为吸热反应,所以正反应为放热反应.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu(0H)2溶于氨水:Cu(0H)2+4NH3=[Cu(NH3)4]2++20H- | |
| B. | 足量的SO2通入Ca(C10)2溶液:Ca2++2C10-+S02═CaS04↓+2C1- | |
| C. | H2S04溶液与Ba(0H)2溶液反应:Ba2++0H-+H++S0${\;}_{4}^{2-}$═BaSO4↓+H20 | |
| D. | NaHC03溶液与过量澄清石灰水反应:2HC0${\;}_{3}^{-}$+Ca2++20H-═CaC03↓+CO${\;}_{3}^{2-}$+2H20 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子中3个碳原子在同一直线上 | |
| B. | 分子中所有原子都在同一平面上 | |
| C. | 分子中共价键的夹角为120° | |
| D. | 分子中共价键数为8,其中有一个碳碳双键 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年重庆市高一上10月月考化学试卷(解析版) 题型:选择题
常温常压下,用等质量的CH4、CO2、O2、SO2四种气体分别吹出四个气球,其中气体为SO2的是
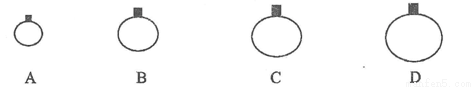
查看答案和解析>>
科目:高中化学 来源:2016-2017学年重庆市高一上10月月考化学试卷(解析版) 题型:选择题
绿色植物是空气天然的“净化器”,研究发现,10000m2柳杉每月可以吸收160kgSO2,则100 m2柳杉每月吸收的SO2的物质的量为
A.2.5mol B.5mol C.25mol D.250mol
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高一上第一次质检化学卷(解析版) 题型:选择题
有一在空气中暴露过的NaOH固体,经分析知其含H2O7.65%,含Na2CO3 4.32%,其余是NaOH。若将ag样品放入bmL1mol/L的盐酸,使其充分作用后,残留酸用25.52mLcmol/L的NaOH溶液恰好中和完全。则蒸发所得溶液,得到固体质量的表达式中(单位为克)
A.应含有a B.只含有b C.比含有c D.一定有a、b、c
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
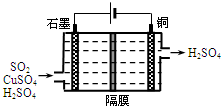 一种以铜作催化剂脱硫有如下两个过程:
一种以铜作催化剂脱硫有如下两个过程:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com