
| A. | 元素X、Z、W各自最高和最低化合价的代数和分别为1、4、6 | |
| B. | 原子半径的大小为Y>Z>W | |
| C. | 元素的非金属性顺序为W>Z>X | |
| D. | Y和其他3种元素均能形成离子化合物 |
分析 X、Y、Z、W是原子序数依次增大的短周期元素,它们的最外层电子数分别为1、1、6、7.X-的电子层结构与氦相同,可知X为H,Y、Z和W的次外层有8个电子,结合最外层电子数可知,Y为Na,Z为S,W为Cl,以此来解答.
解答 解:由上述分析可知,X为H,Y为Na,Z为S,W为Cl,
A.元素X的最高和最低化合价的代数和为+1+(-1)=0,故A错误;
B.同周期从左向右原子半径减小,则原子半径的大小为Y>Z>W,故B正确;
C.同周期从左向右非金属性增强,且氢化物中氢为+1价,元素的非金属性顺序为W>Z>X,故C正确;
D.Na与其它三种元素形成NaH、Na2S、NaCl,均为离子化合物,故D正确;
故选A.
点评 本题考查原子结构与元素周期律,为高频考点,把握原子序数、原子结构来推断元素为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.


 通城学典默写能手系列答案
通城学典默写能手系列答案科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 非金属单质M能从N的化合物中置换出非金属单质N | |
| B. | 在反应中M原子比N原子得到更多电子 | |
| C. | M的气态氢化物稳定性比N弱 | |
| D. | M的氧化物对应水化物的酸性比N强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
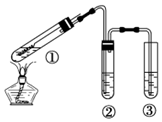
| A. | ②中选用品红溶液验证SO2的生成 | |
| B. | ③中选用NaOH溶液吸收多余的SO2 | |
| C. | 为确认有CuSO4生成,向①中加水,观察颜色 | |
| D. | 上下移动①中铜丝可控制SO2的产生与停止 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验式 CH2 | B. | 结构简式 CH2=CHCH3 | ||
| C. | 球棍模型: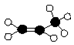 | D. | 加聚反应后的结构简式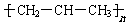 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化硅的分子式为SiO2 | B. | 2-丁烯的键线式: | ||
| C. | 丙烷分子的球棍模型示意图: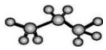 | D. | 乙烯的结构简式:CH2=CH2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com