
| m |
| n |
| 14g |
| 0.5mol |


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
| A、相同温度下,CuS在水中的溶解度比MnS小 |
| B、CuS和MnS一定都溶于强酸 |
| C、反应:Cu2+(aq)+MnS(s)═CuS(s)+Mn2+ K=7.5×1021 |
| D、在浓度均为0.01mol?L-1Cu2+和Mn2+混合溶液中,通入H2S只有MnS沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
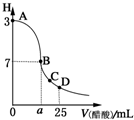 在25mL 0.1mol?L-1NaOH溶液中逐滴加入0.2mol?L-1醋酸溶液,曲线如图所示,有关粒子浓度关系比较不正确的是( )
在25mL 0.1mol?L-1NaOH溶液中逐滴加入0.2mol?L-1醋酸溶液,曲线如图所示,有关粒子浓度关系比较不正确的是( )| A、在D点,c(CH3COO-)+c(CH3COOH)=2c(Na+) |
| B、在C点,c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
| C、在B点,a=12.5,且有c(Na+)=c(CH3COO-)>c(OH-)=c(H+) |
| D、在A、B间任一点,溶液中一定都有c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2 | B、5 | C、9 | D、12 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、已知20℃时,KNO3的溶解度为31.6g.则20℃时KNO3饱和溶液的质量分数等于31.6% |
| B、1mol/L的食盐溶液中含有58.5gNaCl |
| C、所有物质的溶解度随着温度的升高而上升 |
| D、实验室需要230mL 0.1mol/L的H2SO4溶液,应选用250mL容量瓶配制 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、p(H2)>p(O2)>p(Ar) |
| B、p(O2)>p(Ar )>p(H2) |
| C、p(Ar)>p(H2)>p(O2) |
| D、p(H2)>p(Ar)>p(O2) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com