(2010?祁阳县一模)某校化学研究性学习小组为探究铜及其化合物的性质,进行了如下科学探究:
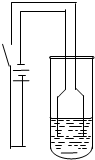
[实验一]:研究性学习小组甲以铜为电极电解饱和食盐水,探究过程如下:
实验过程:按如图装置,接通电源后,阴极产生大量气泡;阳极铜丝由粗变细,不久出现砖红色浑浊,最后在试管底部聚集砖红色沉淀,溶液始终未出现蓝色.
查阅资料:某些铜的化合物有关性质如表所示:
| 物质 |
性质 |
物质 |
性质 |
| 氯化铜 |
浓溶液呈绿色,稀溶液呈蓝色 |
氯化亚铜 |
白色 |
| 氧化亚铜 |
砖红色,在酸性条件下易反应:
Cu2O+2H+=Cu+Cu2++H2O.
Cu2O在空气中灼烧生成CuO |
氢氧化亚铜 |
橙黄色,不稳定 |
请回答下列问题:
(1)试管底部砖红色沉淀的化学式为
Cu2O
Cu2O
.
(2)写出电解总反应方程式
.
[实验二]研究性学习小组乙为检测[实验一]生成的砖红色沉淀中是否含有Cu,设计了以下两种方案进行探究.
方案1:取少量砖红色沉淀溶于足量的浓硝酸中,观察溶液颜色变化.
方案2:取一定质量砖红色沉淀在空气中充分灼烧,根据灼烧前后质量变化进行判断.
(3)请你评价方案1和方案2是否合理,并简述其原因.
方案1
不合理,因为铜和氧化亚铜都能与硝酸生成Cu2+
不合理,因为铜和氧化亚铜都能与硝酸生成Cu2+
.
方案2
合理,因为等质量的Cu2O与Cu2O、Cu的混合物在空气中灼烧前后质量变化不同
合理,因为等质量的Cu2O与Cu2O、Cu的混合物在空气中灼烧前后质量变化不同
.
思考与交流:实验结束后,同学们关于[实验二]中“方案一”溶液呈绿色,而不呈蓝色展开了讨论.丙同学认为是该溶液中硝酸铜的质量分数较高所致;丁同学则认为是该溶液中溶解了生成的气体.
(4)同学们分别设计了以下4个实验来判断两种看法是否正确.这些方案中不可行的是(选填序号字母)
B
B
.
A、加热该绿色溶液,观察颜色变化.
B、加水稀释绿色溶液,观察颜色变化
C、向该绿色溶液中通入氧气,观察颜色变化
D、向饱和的硝酸铜溶液中通入浓硝酸与铜反应产生的气体,观察颜色变化.



 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案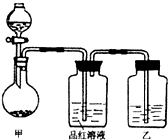 某同学在学习“硫酸及其盐的某些性质与用途“中,进行如下实验探究.
某同学在学习“硫酸及其盐的某些性质与用途“中,进行如下实验探究. CO2↑+2SO2↑+2H2O)
CO2↑+2SO2↑+2H2O) CO2↑+2SO2↑+2H2O)
CO2↑+2SO2↑+2H2O)
 (2010?祁阳县一模)某校化学研究性学习小组为探究铜及其化合物的性质,进行了如下科学探究:
(2010?祁阳县一模)某校化学研究性学习小组为探究铜及其化合物的性质,进行了如下科学探究: 实验室用浓硫酸与铜的反应制取少量 NaHSO3,实验装置如图所示.请回答:
实验室用浓硫酸与铜的反应制取少量 NaHSO3,实验装置如图所示.请回答: 实验室用浓硫酸与铜的反应制取少量NaHSO3,实验装置如图所示:
实验室用浓硫酸与铜的反应制取少量NaHSO3,实验装置如图所示: