
| A. | 乙烯 | B. | 乙二醇 | C. | 乙醇 | D. | 乙酸 |
分析 有机物燃烧完全燃烧生成CO2和H2O,通过足量的石灰水,发生反应:CO2+Ca(OH)2=CaCO3↓+H2O,得到沉淀20g为CaCO3质量,有机物与Na反应生成氢气,含有羟基或羧基,结合生成氢气的体积计算.
解答 解:有机物燃烧产物有二氧化碳和水,将燃烧产物通过足量的石灰水,经过滤可得沉淀20g,应为CaCO3,
n(CO2)=n(CaCO3)=$\frac{20g}{100g/mol}$=0.2mol,
等物质的量的此有机物与足量金属Na反应在标准状况下产生2.24L气体,即n(H2)=$\frac{2.24L}{22.4L/mol}$=0.1mol,应含有羟基或羧基,
由转化关系-OH(-COOH)~H2,可知有机物中C原子数与羟基或羟基的物质的量之比为1:1,
只有乙二醇符合.
故选B.
点评 本题考查有机物的推断,侧重考查学生的分析、计算能力,为高频考点,注意把握物质的性质以及反应的关系,难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 该反应中转移电子数为16NA | |
| B. | 氧化产物与还原产物的粒子个数比为2:5 | |
| C. | 氧化剂与还原剂物质的量之比为1:8 | |
| D. | 氧化剂与还原剂物质的量之比为1:5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO32-、Cl-、OH- | B. | Cl-、CO32-、OH- | C. | OH-、Cl-、CO32- | D. | Cl-、OH-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 向苦卤中通入Cl2前,可先用稀硫酸酸化 | |
| B. | 工业生产中常选用KOH作为沉淀剂 | |
| C. | 粗盐可采用除杂和重结晶等过程提纯 | |
| D. | 富集溴可用热空气吹出单质溴,原因是溴单质沸点低,易挥发 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用溴水检验CH2=CH-CHO中是否含有碳碳双键 | |
| B. | 1mol醛发生银镜反应最多生成2molAg | |
| C. | 对甲基苯甲醛( )使高锰酸钾酸性溶液褪色,说明它含醛基 )使高锰酸钾酸性溶液褪色,说明它含醛基 | |
| D. | 能发生银镜反应的有机物不一定是醛类 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 反应编号 | 反应物质 | 有关现象 |
| ① | A+B | 有沉淀生成 |
| ② | B+C | 有气体放出 |
| ③ | C+D | 有沉淀生成 |
| ④ | B+D | 无明显现象 |
| ⑤ | A+D | 有沉淀生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使紫色石蕊变蓝的溶液:K+、Na+、CH3COO-、SO42- | |
| B. | 含有较多CO32-的溶液中:K+、Fe3+、SO42-、NO3- | |
| C. | 水电离产生的氢离子浓度为10-11mol/L:K+、Ca2+、HCO3-、NO3- | |
| D. | 存在较多的AlO2-的溶液中:Mg2+、Ba2+、Br-、HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{18}^{35}$Cl- | B. | ${\;}_{17}^{35}$Cl | C. | ${\;}_{19}^{35}$Cl- | D. | ${\;}_{17}^{35}$Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
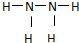 ,过氧化氢的电子式
,过氧化氢的电子式 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com