
·ÖĪö ¢ń£ŗ£Ø1£©ŃĒĮņĖįøłĄė×Ó¾ßÓŠĒæµÄ»¹ŌŠŌ£¬Äܹ»±»ĻõĖįŃõ»ÆÉś³ÉĮņĖįøłĄė×Ó£¬ĻõĖįøłĄė×Ó±»»¹ŌĪŖŅ»Ńõ»ÆµŖ£¬SŌŖĖŲÓÉ+4¼ŪÉżøßµ½+6¼Ū£¬NŌŖĖŲÓÉ+5¼Ū½µµĶµ½+2¼Ū£¬ŅĄ¾Ż»ÆŗĻ¼ŪÉż½µŹżĻąĶ¬½įŗĻŌ×ÓøöŹżŹŲŗ抓³ö·½³ĢŹ½£»
£Ø2£©Čō·“Ó¦ŗ󣬻¹Ō²śĪļµÄ»ÆŗĻ¼Ū½µµĶ£¬¶ųĘäĖūĪļÖŹ¼ŪĢ¬±£³Ö²»±ä£¬ŠčŅŖµÄŃõ»Æ¼ĮµÄĪļÖŹµÄĮæĘ«Š”£»
¢ņ£ŗ£Ø1£©ŅĄ¾ŻÅäÖĘŅ»¶ØĪļÖŹµÄĮæÅضČČÜŅŗµÄŅ»°ć²½ÖčŃ”ŌńŗĻŹŹµÄŅĒĘ÷£»
£Ø3£©ŅĄ¾Żm=CVM¼ĘĖćŠčŅŖČÜÖŹµÄÖŹĮ棻
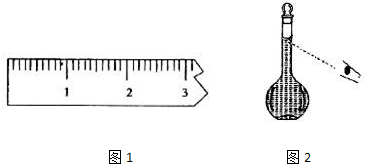
¢Ł³ĘĮæŹ±Šč·ÅŅ»øö5gµÄķĄĀė£¬2.2gŠčµ÷ÓĪĀė£»
£Ø4£©ŅĄ¾Ż²£Į§°ōŌŚČܽā¹ĢĢåŹ±×÷ÓĆ½ā“š£»
£Ø5£©ŃöŹÓæĢ¶ČĻߣ¬µ¼ÖĀČÜŅŗµÄĢå»żĘ«“ó£®
½ā“š ½ā£ŗ¢ń£Ø1£©ŃĒĮņĖįøłĄė×Ó¾ßÓŠĒæµÄ»¹ŌŠŌ£¬ŌŚĖįŠŌ»·¾³ĻĀÓėĻõĖįøłĄė×Ó·¢Éś·“Ӧɜ³ÉĮņĖįøłĄė×Ó”¢¶žŃõ»ÆµŖŗĶĖ®£¬Ąė×Ó·½³ĢŹ½ĪŖ£ŗ2H++2NO3-+3SO32-=3SO42-+2NO”ü+H2O£»
£Ø2£©Čō·“Ó¦ŗ󣬻¹Ō²śĪļµÄ»ÆŗĻ¼Ū½µµĶ£¬¶ųĘäĖūĪļÖŹ¼ŪĢ¬±£³Ö²»±ä£¬ŠčŅŖµÄŃõ»Æ¼ĮµÄĪļÖŹµÄĮæĘ«Š”£¬Ōņ·“Ó¦ÖŠŃõ»Æ¼ĮÓė»¹Ō¼ĮµÄĪļÖŹµÄĮæÖ®±Č½«¼õŠ”£»
¹Ź“š°øĪŖ£ŗ¼õŠ”£»
¢ņ£ŗ£Ø1£©ÅäÖĘ0.10mol/L Na2CO3ČÜŅŗµÄŅ»°ć²½ÖčĪŖ£ŗ¼ĘĖć”¢³ĘĮ攢Čܽā”¢ĄäČ“”¢ŅĘŅŗ”¢Ļ“µÓ”¢¶ØČŻ”¢Ņ”ŌČµČ£¬ŠčŅŖŹ¹ÓƵÄŅŖĒóĪŖ£ŗÉÕ±”¢²£Į§°ō”¢½ŗĶ·µĪ¹Ü”¢250mLČŻĮæĘ棬»¹Č±ÉŁµÄŅĒĘ÷ĪŖ£ŗ½ŗĶ·µĪ¹Ü”¢250mLČŻĮæĘ棻
¹Ź“š°øĪŖ£ŗ250mLČŻĮæĘ棻½ŗĶ·µĪ¹Ü£»
£Ø3£©ÅäÖĘ0.10mol/L Na2CO3ČÜŅŗ240mL£¬Ó¦Ń”Ōń250mlČŻĮæĘ棬ŠčŅŖNa2CO3•10H2OµÄÖŹĮæm=0.10mol/L”Į0.25L”Į286g/mol=7.2g£¬¹Ź“š°øĪŖ£ŗ7.2£»
¢Ł³ĘĮæŹ±Šč·ÅŅ»øö5gµÄķĄĀė£¬2.2gŠčµ÷ÓĪĀė£¬ČēĶ¼ĖłŹ¾£ŗ £¬¹Ź“š°øĪŖ£ŗ
£¬¹Ź“š°øĪŖ£ŗ £»
£»
£Ø4£©ĪŖ¼ÓæģČܽāŗĶĄäČ“ĖŁ¶Č£¬ŌŚČܽā”¢ĄäČ“Ź±ŠčÓĆ²£Į§°ō²»¶ĻµÄ½Į°č£¬¹Ź“š°øĪŖ£ŗ½Į°č£¬¼ÓĖŁČܽāŗĶĄäČ“£»
£Ø5£©ŃöŹÓæĢ¶ČĻߣ¬µ¼ÖĀČÜŅŗµÄĢå»żĘ«“ó£¬ŅĄ¾ŻC=$\frac{n}{V}$æÉÖŖ£¬ČÜŅŗµÄĢå»żĘ«“ó£¬ČÜŅŗµÄÅضČĘ«µĶ£¬¹Ź“š°øĪŖ£ŗĘ«µĶ£®
µćĘĄ ±¾Ģāæ¼²éĮĖŃõ»Æ»¹ŌøÅÄī¼°·½³ĢŹ½µÄŹéŠ“£¬ÅäÖĘŅ»¶ØĪļÖŹµÄĮæÅضČČÜŅŗ£¬Ć÷Č·Ńõ»Æ»¹Ō·“Ó¦¹ęĀɼ°ÅäÖĘŅ»¶ØĪļÖŹµÄĮæÅضČČÜŅŗµÄŌĄķŹĒ½āĢā¹Ų¼ü£¬×¢ŅāĶŠÅĢĢģĘ½µÄÕżČ·Ź¹ÓĆ·½·Ø£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
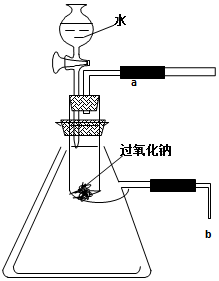 ÓĆĶŃ֬Ǝ°ü×”0.39g¹żŃõ»ÆÄĘ·ŪÄ©£¬ÖĆÓŚŹÆĆŽĶųÉĻ£¬ĶłĶŃ֬ƎÉĻµĪ¼øµĪĖ®£¬æɹŪ²ģµ½ĶŃ֬Ǝ¾ēĮŅČ¼ÉÕĘšĄ“£®
ÓĆĶŃ֬Ǝ°ü×”0.39g¹żŃõ»ÆÄĘ·ŪÄ©£¬ÖĆÓŚŹÆĆŽĶųÉĻ£¬ĶłĶŃ֬ƎÉĻµĪ¼øµĪĖ®£¬æɹŪ²ģµ½ĶŃ֬Ǝ¾ēĮŅČ¼ÉÕĘšĄ“£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ×Ŗ»Æ¢ŁÓŠĄūÓŚĢ¼²ĪÓė×ŌČ»½ēµÄŌŖĖŲŃ»· | |
| B£® | ×Ŗ»Æ¢ŚÖŠSŗĶO2ŹōÓŚ²»Ķ¬µÄŗĖĖŲ | |
| C£® | æÉÓĆ³ĪĒåµÄŹÆ»ŅĖ®¼ų±šCO2ÓėSO2 | |
| D£® | ×Ŗ»ÆµÄČČ»Æѧ·½³ĢŹ½ŹĒ£ŗ2CO£Øg£©+SO2£Øg£©ØTS£Øs£©+2CO2 £Øg£©”÷H=+270kJ/mol |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
| ĪļÖŹ | ×é³ÉŗĶ½į¹¹ŠÅĻ¢ |
| a | ŗ¬ÓŠAµÄ¶žŌŖĄė×Ó»ÆŗĻĪļ |
| b | ŗ¬ÓŠ·Ē¼«ŠŌ¹²¼Ū¼üµÄ¶žŌŖĄė×Ó»ÆŗĻĪļ£¬ĒŅŌ×ÓŹżÖ®±ČĪŖ1£ŗ1 |
| c | »Æѧ×é³ÉĪŖBDF2 |
| d | Ö»“ęŌŚŅ»ÖÖĄąŠĶ×÷ÓĆĮ¦ĒŅæɵ¼µēµÄµ„ÖŹ¾§Ģå |
 £»dµÄ¾§ĢåĄąŠĶŹĒ½šŹō£®
£»dµÄ¾§ĢåĄąŠĶŹĒ½šŹō£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® |  | B£® |  | C£® |  | D£® |  |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¼ĘĖćĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ±źæöĻĀ£¬11.2L ·ś»ÆĒāÖŠŗ¬ÓŠµÄ·Ö×ÓŹżÄæĪŖ0.5NA | |
| B£® | ŹŅĪĀĻĀ£¬21.0gŅŅĻ©ŗĶ¶”Ļ©µÄ»ģŗĻĘųĢåÖŠĖłŗ¬µÄĢ¼Ō×ÓŹżÄæŹĒNA | |
| C£® | ŹŅĪĀĻĀ£¬2L0.05mol/L µÄNH4NO3ČÜŅŗÖŠĖłŗ¬ÓŠµÄµŖŌ×ÓŹżÄæŹĒ0.2NA | |
| D£® | 22.4L Cl2 Óė×ćĮæNaOHČÜŅŗ·“Ó¦Ź±×ŖŅʵĵē×ÓŹżĪŖNA |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com