
【题目】从樟科植物枝叶提取的精油中含有甲、乙两种成分:
![]()
(1)乙中含官能团的名称为_______和______________。
(2)由甲转化为乙的过程为(已略去无关产物):
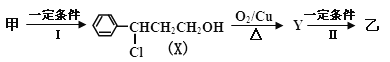
①反应II 的反应类型为____________,Y的结构简式___________________。
②设计步骤I的目的是___________________________________________________________。
(3)按顺序写出检验X中卤素原子所需的试剂________________________________。
(4)写出乙与新制Cu (OH)2悬浊液反应的化学方程式______________________________。
(5) 乙经过氧化得到丙(![]() )写出同时符合下列要求的丙的同分异构体的结构简式_____________________、_______________________。
)写出同时符合下列要求的丙的同分异构体的结构简式_____________________、_______________________。
① 能发生银镜反应②遇FeCl3溶液显色③核磁共振氢谱显色有4 种氢
【答案】 醛基 碳碳双键 消去反应 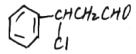 保护碳碳双键 NaOH溶液、稀HNO3、AgNO3溶液
保护碳碳双键 NaOH溶液、稀HNO3、AgNO3溶液 ![]()
【解析】(1)根据有机物乙的结构简式可知,其所含官能团的名称为醛基、碳碳双键;正确答案:醛基、碳碳双键。
(2)①由物质的结构可以知道,反应Ⅰ是甲中碳碳双键与HCl发生加成反应生成![]() ,然后
,然后![]() 中醇羟基发生氧化反应生成Y为
中醇羟基发生氧化反应生成Y为![]() ,反应Ⅱ是Y发生卤代烃的消去反应生成乙;正确答案:消去反应;
,反应Ⅱ是Y发生卤代烃的消去反应生成乙;正确答案:消去反应;![]() 。
。
②有机物甲中含有碳碳双键和羟基,若直接用氧化剂把羟基氧化为醛基时,碳碳双键也易被氧化,所以设计步骤I的目的是保护碳碳双键;正确答案:保护碳碳双键。
(3)有机物X在氢氧化钠溶液中加热反应生成醇和氯化钠,然后向反应后的混合液中加入足量的稀硝酸,中和氢氧化钠溶液,然后向中和后的溶液中加入硝酸银溶液,如果有白色沉淀产生,证明该卤代烃为氯代烃;正确的选用试剂顺序为NaOH溶液、稀HNO3、AgNO3溶液;正确答案:NaOH溶液、稀HNO3、AgNO3溶液。
(4)醛基能够被Cu(OH)2悬浊液氧化为羧基,本身还原为氧化亚铜;反应的化学方程式:![]() ;正确答案:
;正确答案:![]() 。
。
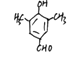
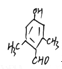
(5)分子式为C9H10O2,①能发生银镜反应,含有醛基;②遇FeCl3溶液显色,含有酚羟基;③核磁共振氢谱显色有4种氢,即有4种峰;满足上述条件的有机物有2种 ,分别为: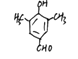 、
、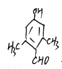 ;正确答案:
;正确答案: 、
、 。
。


 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案 品学双优卷系列答案
品学双优卷系列答案科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E五种元素,其中A、B、C属于同一周期,A原子最外层p轨道的电子数等于次外层的电子总数,B元素可分别与A、C、D、E生成RB2型化合物,并知在DB2和EB2中,D与B的质量比为7∶8,E与B的质量比为1∶1。根据以上条件,回答下列问题:
(1)画出C的原子结构示意图:________。
(2)写出D原子的外围电子排布式:________。
(3)写出A元素单质在B中完全燃烧的化学方程式:______________。
(4)指出E元素在元素周期表中的位置:____________。
(5)比较A、B、C三种元素的第一电离能的大小顺序:________________(按由大到小的顺序排列,用元素符号表示)。
(6)比较元素D和E的电负性的相对大小:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究表明,氮氧化物和二氧化硫在形成雾霾时与大气中的氨有关(如下图所示)。下列叙述错误的是

A. 雾和霾的分散剂相同
B. 雾霾中含有硝酸铵和硫酸铵
C. NH3是形成无机颗粒物的催化剂
D. 雾霾的形成与过度施用氮肥有关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向CuSO4溶液中逐滴加入KI溶液至过量,观察到产生白色沉淀CuI,溶液变为棕色。再向反应后的混合物中不断通入SO2气体,溶液逐渐变成无色。下列分析正确的是( )
A. 上述实验条件下,物质的氧化性:Cu2+>I2>SO2
B. 通入SO2时,SO2与I2反应,I2作还原剂
C. 通入SO2与I2反应,I2作还原剂后溶液逐渐变成无色,体现了SO2的漂白性
D. 滴加KI溶液时,转移2 mol电子时生成1 mol白色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数的值。下列说法正确的是
A. 常温常压下,124 g P4中所含P—P键数目为4NA
B. 100 mL 1mol·L1FeCl3溶液中所含Fe3+的数目为0.1NA
C. 标准状况下,11.2 L甲烷和乙烯混合物中含氢原子数目为2NA
D. 密闭容器中,2 mol SO2和1 mol O2催化反应后分子总数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是一个电化学过程的示意图,回答下列问题:

(1)甲池将______能转化为______能,乙装置中电极A是____极。
(2)甲装置中通入CH4的电极反应式为__________________________________,乙装置中电极B(Ag)的电极反应式为________________________________。
(3)一段时间,当丙池中产生112 mL(标准状况)气体时,均匀搅拌丙池,所得溶液在25 ℃时的pH=________(已知:NaCl溶液足量,电解后溶液体积为500 mL)。若要使丙池恢复电解前的状态,应向丙池中通入________(写化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中A为278g/mol。B、D、E、F、G是氧化物且B为红棕色固体,F、K是氢化物,C、H是日常生活中最常见的金属单质,J是黄绿色气体。O是白色沉淀(图中部分反应物和生成物没有列出)。

(1)写出A、G、L的化学式A______________:G: _______________,L:______________。
(2)反应②的化学方程式 ________________________________________________。
(3)写出反应M→L的离子方程式为________________________________________。
(4)若将O敞口久置,变质过程中的现象为___________________________________,发生的化学方程式为__________________________________________________。
(5)向M溶液中投入与M等物质的量的Na2O2,反应的离子方程式是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,5种银盐的溶度积常数(Ksp)分别是:
AgCl | Ag2SO4 | Ag2S | AgBr | AgI |
1.8×10-10 | 1.4×10-5 | 6.3×10-50 | 7.7×10-13 | 8.51×10-16 |
下列说法正确的是
A. 氯化银、溴化银和碘化银的溶解度依次增大
B. 将硫酸银溶解于水后,向其中加入少量硫化钠固体,不能得到黑色沉淀
C. 在5mL1.5×10-5molL-1的NaCl溶液中,加入1滴(1mL约20滴)1.0×10-3molL-1的AgNO3溶液,不能观察到白色沉淀
D. 在烧杯中放入6.24 g硫酸银固体,加200 g 水,经充分溶解后,所得饱和溶液的体积为200 mL,溶液中Ag + 的物质的量浓度为0.2molL-1。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com