
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
| A. | 当v逆(X)=2v正(Z),可以说明反应达平衡 | |
| B. | 反应前2 min的平均速率v(Z)=4.0×10?3 mol•L?1•min?1 | |
| C. | 其他条件不变,再充入0.2 mol Z,平衡时X的体积分数增大 | |
| D. | 该反应在350℃时的平衡常数小于1.44 |
分析 A.不同物质表示的正逆速率之比等于其化学计量数之比,可逆反应到达平衡;
B.根据v=$\frac{△c}{△t}$计算2min内Y表示的反应速率,再利用速率之比等于化学计量数之比计算v(Z);
C.其他条件不变,再充入0.2 mol Z,等效为压强增大到达的平衡,反应前后气体体积不变,增大压强平衡不移动;
D.由表中数据可知,7min与9min时Y的物质的量相等,说明7min时到达平衡,利用三段式计算平衡时各组分物质的量,由于反应气体体积不变,用物质的量代替浓度代入平衡常数表达式K=$\frac{{c}^{2}(Z)}{c(X)×c(Y)}$,计算300℃时平衡常数,该反应为放热反应,升高温度,平衡向逆反应方向移动,平衡常数减小.
解答 解:A.当v逆(X)=2v正(Z),则v逆(X):v正(Z)=2:1,不等于其化学计量数之比1:2,故A错误;
B.由表中数据可知,2min内参加反应的Y为0.16mol-0.12mol=0.04mol,则v(Y)=$\frac{\frac{0.04mol}{10L}}{2min}$=2.0×10?3 mol•L?1•min?1,速率之比等于化学计量数之比,v(Z)=2v(Y)=4.0×10?3 mol•L?1•min?1,故B正确;
C.其他条件不变,再充入0.2 mol Z,等效为压强增大到达的平衡,反应前后气体体积不变,增大压强平衡不移动,平衡时X的体积分数不变,故C错误;
D.由表中数据可知,7min与9min时Y的物质的量相等,说明7min时到达平衡,
X(g)+Y(g)?2Z(g)
开始(mol):0.16 0.16 0
转化(mol):0.06 0.06 0.12
平衡(mol):0.1 0.1 0.12
由于反应气体体积不变,用物质的量代替浓度计算平衡常数,故300℃时平衡常数K=$\frac{{c}^{2}(Z)}{c(X)×c(Y)}$=$\frac{0.1{2}^{2}}{0.1×0.1}$=1.44,该反应为放热反应,升高温度,平衡向逆反应方向移动,平衡常数减小,即该反应在350℃时的平衡常数小于1.44,故D正确,
故选:BD.
点评 本题考查化学反应速率计算、化学平衡计算、等效平衡、化学平衡常数计算及影响因素等,C选项注意利用等效平衡分析解答,也可以利用借助平衡常数理解,难度中等.


 高中必刷题系列答案
高中必刷题系列答案科目:高中化学 来源: 题型:选择题
| A. | 溴苯中混有溴,加入KI溶液,用汽油萃取出溴 | |
| B. | 乙烷中混有乙烯,在一定条件下反应通入氢气,使乙烯转化为乙烷 | |
| C. | 硝基苯中混有浓硝酸和浓硫酸,将其倒入浓烧碱溶液中,静置,然后分液 | |
| D. | 乙烷中混有CO2,将其通入碳酸氢钠溶液洗气后干燥 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
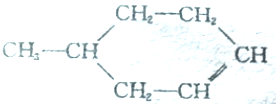 可以写成
可以写成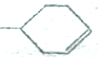 ,现有有机物A,可写为
,现有有机物A,可写为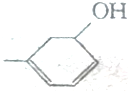
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
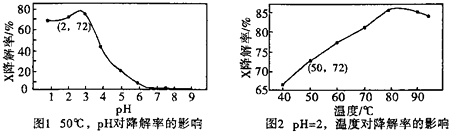
| A. | pH=2、温度为50℃、10 min时,X的物质的量浓度c( X)为5.6×10-4mol•L-1 | |
| B. | 图2说明:任何条件下X降解率均随温度升高先增后减 | |
| C. | 无需再进行后续实验,就可以判断最佳反应条件是:pH=3、温度为80℃ | |
| D. | 图1说明:50℃时,X的降解率随溶液PH的增大而逐渐减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
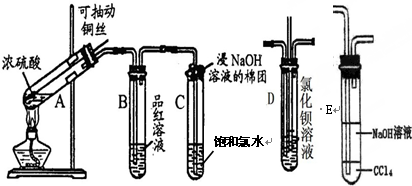
| 资料1 | 硫酸浓度mol/L | 黑色物质出现的温度∕℃ | 黑色物质消失的温度∕℃ |
| 15 | 约150 | 约236 | |
| 16 | 约140 | 约250 | |
| 18 | 约120 | 不消失 | |
| 资料2 | X射线衍射晶体分析表明,铜与浓硫酸反应生成的黑色物质为Cu2S、CuS、Cu7S4中的一种或几种. | ||
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{2}^{3}$He代表原子核内有2个质子和3个中子的氦原子 | |
| B. | ${\;}_{2}^{3}$He和${\;}_{2}^{4}$He分别含有1和2个质子 | |
| C. | ${\;}_{2}^{3}$He 和${\;}_{2}^{4}$He互为同位素 | |
| D. | ${\;}_{2}^{3}$He的最外层电子数为1,所以${\;}_{2}^{3}$He 具有较强的金属性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
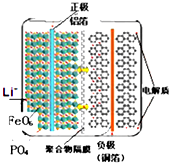
| A. | 放电时,铝箔所在电极为负极,铜箔所在电极为正极 | |
| B. | 放电时,电池反应式为:FePO4+Li═LiFePO4 | |
| C. | 充电时,Li+向阴极移动 | |
| D. | 充电时,阳极的电极反应式为:LiFePO4-e-═FePO4+Li+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ③④ | C. | ①④ | D. | ②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
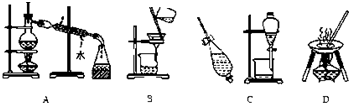
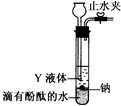
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com