
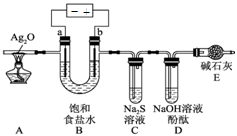


科目:高中化学 来源:不详 题型:单选题
| A.电解稀硫酸溶液,溶液的浓度会逐渐变大,pH逐渐变大 |
| B.氯碱工业中,电路中每转移1mol电子,理论上收集到1mol气体 |
| C.向电解氯化钠溶液所得的稀溶液中,加入浓盐酸,能恢复到原溶液浓度 |
| D.粗铜精炼时,粗铜应作电解池的阳极,电解质溶液在电解过程中浓度不变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
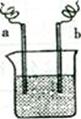
| A.该装置可能是电解池 |
| B.a极上发生的是还原反应 |
| C.a、b不可能是同种电极材料 |
| D.该装置工作时,溶液中的阴离子向b极移动 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.2Cl-+Cu2+ Cu+Cl2↑ Cu+Cl2↑ |
B.2Cl-+2H2O H2↑+Cl2↑+2OH- H2↑+Cl2↑+2OH- |
C.2Cu2++2H2O 2Cu+O2↑+4H+ 2Cu+O2↑+4H+ |
D.2H2O 2H2↑+O2↑ 2H2↑+O2↑ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

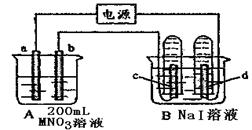
| A.甲池b极上析出金属银,乙池c极上析出某金属 |
| B.甲池a极上析出金属银,乙池d极上析出某金属 |
| C.某盐溶液可能是CuSO4溶液 |
| D.某盐溶液可能是Mg(NO3)2溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
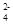 中选取适当的离子组成符合下列情况的电解质,进行电解(阳离子只能使用一次)。
中选取适当的离子组成符合下列情况的电解质,进行电解(阳离子只能使用一次)。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com