
分析 NO、H2、CO2混合气体在过量Na2O2的添加下用电火花点燃,生成70%的HNO3,设生成70gHNO3,则n(HNO3)=$\frac{70g}{63g/mol}$=1.1mol,n(H2O)=$\frac{30g}{18g/mol}$=1.67mol,结合反应2CO2+2Na2O2=2Na2CO3+O2,2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O,4NO+3O2+2H2O=4HNO3计算该题.
解答 解:NO、H2、CO2混合气体在过量Na2O2的添加下用电火花点燃,生成70%的HNO3,设生成70gHNO3,则n(HNO3)=$\frac{70g}{63g/mol}$=1.1mol,n(H2O)=$\frac{30g}{18g/mol}$=1.67mol,
有质量守恒可知n(NO)=n(HNO3)=1.1mol,
n(H2)=n(H2O)+$\frac{1}{2}$n(HNO3)=2.22mol,
发生2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O,4NO+3O2+2H2O=4HNO3,则共需要n(O2)=$\frac{1}{2}$n(H2)+$\frac{3}{4}$n(NO)=1.11mol+0.825mol=1.935mol,
则由2CO2+2Na2O2=2Na2CO3+O2可知n(CO2)=3.87mol,
n(NO):n(H2):n(C02)=1.1:2.22:3.87=1:2:3.5,
故答案为:1:2:3.5.
点评 本题考查混合物的计算,为高频考点,侧重于学生的分析能力和计算能力的考查,注意把握反应的方程式,结合方程式计算该题,难度中等.


科目:高中化学 来源: 题型:选择题

| A. | X如果是硫酸铜,a和b分别连接直流电源正、负极,一段时间后铁片质量增加 | |
| B. | X如果是氯化钠,则a和b连接时,该装置可模拟生铁在食盐水中被腐蚀的过程 | |
| C. | X如果是硫酸铁,则不论a和b是否用导线连接,铁片均发生氧化反应 | |
| D. | X如果是氢氧化钠,将碳电极改为铝电极,a和b用导线连接,此时构成原电池铁作负极 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
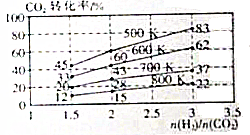 二氧化碳是造成温室效应的主要气体,二氧化碳的回收在利用是减缓温室效应的有效途径之一.
二氧化碳是造成温室效应的主要气体,二氧化碳的回收在利用是减缓温室效应的有效途径之一.| 温度/K CO2转化率/% a/mol | 500 | 600 | 700 | 800 |
| 1.67 | x | 33 | ||
| 1.25 | 60 | 43 | y | |
| 0.83 | z | 32 | w |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 正极反应为2CO2+O2+4e-═2CO32- | |
| B. | CO32-向正极移动 | |
| C. | 电子由正极经外电路流向负极 | |
| D. | 电池中CO32-的物质的量将逐渐减少 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④⑤⑥ | B. | ②④⑤⑥ | C. | ①②③⑤ | D. | ③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
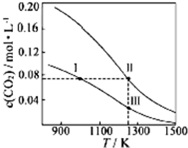 在体积均为1.0L的量恒容密闭容器中加入足量的相同的碳粉,再分别加入0.1molCO2和0.2molCO2,在不同温度下反应CO2(g)+C(s)?2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上).下列说法正确的是( )
在体积均为1.0L的量恒容密闭容器中加入足量的相同的碳粉,再分别加入0.1molCO2和0.2molCO2,在不同温度下反应CO2(g)+C(s)?2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上).下列说法正确的是( )| A. | 反应CO2(g)+C(s)?2CO(g)的△S>0、△H<0 | |
| B. | 体系的总压强P总:P总(状态Ⅱ)>2P总(状态Ⅰ) | |
| C. | 体系中c(CO):c(CO,状态Ⅱ)<2c(CO,状态Ⅲ) | |
| D. | 逆反应速率V逆:V逆(状态Ⅰ)>V逆(状态Ⅲ) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl2、Al、H2 | B. | F2、K、HCl | C. | NO2、Na、Br2 | D. | HNO3、SO2、H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙酸与乙酸乙酯的混合物,可通过蒸馏或用足量饱和碳酸钠溶液洗涤后分液的方法进行分离 | |
| B. | 做金属钠和水反应实验时,切割下来的表层物质,也不能直接丢弃到废纸篓里,而应放回原试剂瓶 | |
| C. | 酸式滴定管在润洗时,可在滴定管中加入少量待装液,润洗后将溶液从滴定管的上口倒入废液缸中,重复2~3次,润洗完毕 | |
| D. | 高锰酸钾是一种常用的化学试剂,当高锰酸钾晶体结块时,应在研钵中用力研磨,以得到细小晶体,有利于加快反应或溶解的速率 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com