
根据离子方程式:①2Fe3++2I―=2Fe2++I2;②2Fe2++Br2=2Fe3++2Br―,判断有关离子的还原性由弱到强的顺序是( )
A.Br―<Fe2+<I― B.I―<Fe2+<Br― C.Br―<I―<Fe2+ D.Fe2+<Br―<I―
科目:高中化学 来源: 题型:

 2Ag+4NH3+CH2OH(CHOH)4COOH+H2O
2Ag+4NH3+CH2OH(CHOH)4COOH+H2O 2Ag+4NH3+CH2OH(CHOH)4COOH+H2O
2Ag+4NH3+CH2OH(CHOH)4COOH+H2O查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
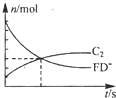 短周期元素A-F的原子序数依次增大,部分元素的信息如下:
短周期元素A-F的原子序数依次增大,部分元素的信息如下:| 元素编号 | 信息 |
| B | 与元素A、D共同组成的化合物的种类最多 |
| D | 最外层电子数是次外层电子数的三倍 |
| E | 同周期元素中形成的简单离子半径最小 |
| F | 最高价氧化物对应的水化物的酸性最强 |
| 编号 | 性质 | 化学方程式 |
| 示例 | 氧化性 | H2WO3+3H3PO3=3H3PO4+H2W↑ |
| ① | ||
| ② |
查看答案和解析>>
科目:高中化学 来源: 题型:
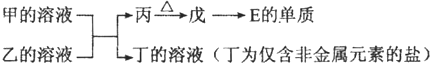
根据离子方程式写出一个符合条件的化学方程式
(1)CO2+2OH-=CO32-+H2O
(2)H++OH-=H2O
(3)BaCO3+2H+=Ba2++CO2↑+H2O
(4)Ca2++CO32-=CaCO3↓
查看答案和解析>>
科目:高中化学 来源:2015届贵州省高二上学期期中考试理科化学试卷(解析版) 题型:填空题
Ⅰ.课本中通过向草酸(H2C2O4)溶液中滴加用硫酸酸化高锰酸钾中研究浓度对化学反应速率的影响,请你写出该反应的化学方程式 ,该反应不需使用指示剂的原因是 ;
Ⅱ.某同学根据课本外界条件对化学反应速率的影响原理,设计了硫代硫酸钠与硫酸反应有关实验,实验过程的数据记录如下(见表格),请结合表中信息,回答有关问题:
实验
序号 反应温度
(℃) 参加反应的物质
Na2S2O3 H2SO4 H2O
V/mL c/mol•L-1 V/mL c/mol•L-1 V/mL
A 20 10 0.1 10 0.1 0
B 20 5 0.1 10 0.1 5
C 20 10 0.1 5 0.1 5
D 40 5 0.1 10 0.1 5
(1)写出上述反应的离子方程式
(2)根据你所掌握的知识判断,在上述实验中反应速率最快的可能是 (填实验序号)
(3)在利用比较某一因素对实验产生的影响时,必须排除其他因素的变动和干扰,即需要控制好与实验有 关的各项反应条件.其中:
①能说明温度对该反应速率影响的组合比较是 ;(填实验序号)
②A和B、A和C的组合比较所研究的问题是
③B和C的组合比较所研究的问题是
(4)教材是利用了出现黄色沉淀的快慢来比较反应速率的快慢,请你分析为何不采用排水法测量单位时间内气体体积的大小的可能原因:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com