
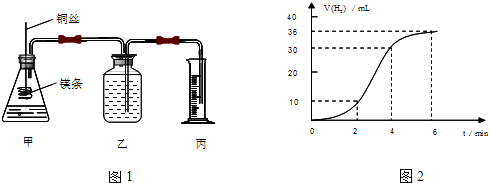
分析 (1)镁与盐酸反应生成氯化镁和氢气,据此写出反应的离子方程式;
(2)分析相同时间内氢气体积的多少来判断速率的快慢;
(3)先根据图2找出2、4、6min时刻时的氢气体积的变化量,再找出2、4、6min时刻时的速率与时间的关系,然后用平滑曲线描绘图象.
(4)在前4min内,该反应放热热量,温度升高导致反应速率加快;4min后由于溶液中H+浓度降低,导致反应速率减小.
解答 解:(1))镁与盐酸反应生成氯化镁和氢气,反应的离子方程式为:Mg+2H+═Mg2++H2↑,
故答案为:Mg+2H+═Mg2++H2↑;
(2)从图中看出2-4分钟内产生氢气最多,故这段时间内反应速率最大,
故答案为:B;
(3)2、4、6min时刻时氢气体积的分别为10 mL、20mL、36mL,其平均反应速率分别为5 mL/min、7.5mL/min、6mL/min,然后标出速率与时间图象为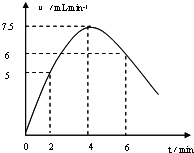 ,
,
故答案为: ;
;
(4)在前4min内,镁条与盐酸的反应速率逐渐加快,原因是镁和盐酸反应是放热反应,随着反应体系温度升高,反应速率增大;
在4min之后,反应速率逐渐减慢,原因是4min后由于溶液中H+浓度降低,浓度越小反应速率越小,所以导致反应速率减小,
故答案为:镁和盐酸反应是放热反应,随着反应体系温度升高,反应速率增大;4min后由于溶液中H+浓度降低,所以导致反应速率减小.
点评 本题考查了影响化学反应速率因素,题目难度中等,试题侧重于学生的分析能力和实验能力的考查,为高考常见题型,明确温度、浓度等因素对化学反应速率的影响为解答关键.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
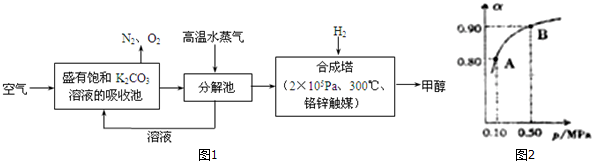
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化石燃料燃烧和工业废气中的氮氧化物均是导致“雾霾天气”的元凶 | |
| B. | 天津港爆炸事件中可知,当电石、钠、氰化钠等物品遇到明火时,应迅速用水浇灭 | |
| C. | 新发现一种固态碳,外形似海绵,密度小,有磁性,其与金刚石的关系是同素异形体 | |
| D. | 热的纯碱溶液去除厨房油污效果比冷的纯碱溶液效果好 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室用大理石跟稀盐酸制取二氧化碳:2H++CO32-═CO2↑+H2O | |
| B. | 氯化铝中加入氨水:Al3++3OH-═Al(OH)3↓ | |
| C. | 铁粉与氯化铁溶液反应:Fe+Fe3+═2Fe2+ | |
| D. | 硫酸铜与氢氧化钡溶液反应:Cu2++SO42-+Ba2++2OH-═Cu(OH)2↓+BaSO4↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
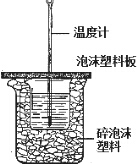 用如图所示装置进行中和热测定实验,请回答下列问题:
用如图所示装置进行中和热测定实验,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com