
下列反应属于取代反应的是( )
A.C2H4+3O2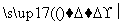 2CO2+2H2O
2CO2+2H2O
B.Zn+CuSO4===ZnSO4+Cu
C.NaCl+AgNO3===AgCl↓+NaNO3
D.CH2Cl2+Cl2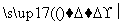 CHCl3+HCl
CHCl3+HCl
科目:高中化学 来源: 题型:
现有一样品,经分析含氧化钙、碳酸钙两种物质。向该样品中加入溶质质量分数为7.3%的稀盐酸100g,恰好完全反应得到溶液,(已知CaO + 2HCl = CaCl2 + H2O),蒸干该溶液得到固体质量为
A.11.1g B.22.2g C.7.3g D.14.6g
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学在学习等径球最密堆积(立方最密堆积A1和六方最密堆积A3)后,提出了另一种最密堆积形式Ax 。如右图所示为Ax 堆积的片层形式,然后第二层就堆积在第一层的空隙上。请根据Ax 的堆积形式回答:
(1)计算在片层结构中(如右图所示)球数、空隙数和切点数之比
(2)在Ax 堆积中将会形成正八面体空隙和正四面体空隙。请在片层图中画出正八面体空隙(用·表示)和正四面体空隙(用×表示)的投影,并确定球数、正八面体空隙数和正四面体空隙数之比
(3)指出Ax 堆积中小球的配位数
(4)计算Ax 堆积的原子空间利用率。
(5)计算正八面体和正四面体空隙半径(可填充小球的最大半径,设等径小球的半径为r)。
(6)已知金属Ni晶体结构为Ax 堆积形式,Ni原子半径为124.6 pm,计算金属Ni的密度。(Ni的相对原子质量为58.70)
(7)如果CuH 晶体中Cu+的堆积形式为Ax 型,H- 填充在空隙中,且配位数是4。则H- 填充的是哪一类空隙,占有率是多少?
(8)当该同学将这种Ax 堆积形式告诉老师时,老师说Ax 就是A1或A3的某一种。你认为是哪一种,为什么?
查看答案和解析>>
科目:高中化学 来源: 题型:
核电荷数小于18的某元素X,其原子的电子层数为n,最外层电子数为2n+1,原子核内质子数是2n2-1。下列有关元素X的说法中不正确的是( )
A.元素X能形成化学式为X(OH)3的碱
B.元素X可能形成化学式为KXO3的含氧酸钾盐
C.元素X原子的最外层电子数和核电荷数肯定为奇数
D.元素X能与某些金属元素形成化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示,U形管的左端被水和胶塞封闭,充有甲烷和氯气(体积比为14)的混合气体,假定氯气在水中的溶解可以忽略不计。将封闭有甲烷和氯气的混合气体的装置放置在有光亮的地方,让混合气体缓慢地反应一段时间。
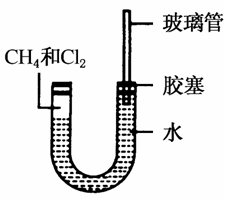
(1)假设甲烷与氯气充分反应,且只生成一种有机物,请写出该反应的化学方程式________________________________________。
(2)经过几个小时的反应后,U形管右端的水面变化是________________________________________________________。
A.升高 B.降低
C.不变 D.无法确定
(3)U形管左端的气柱变化是________。
A.体积增大 B.体积减小
C.消失 D.不变
(4)U形管右端的水面变化的原因_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在烷烃分子中的基团: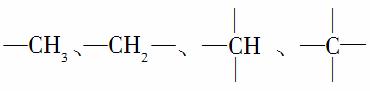 中的碳原子分别称为伯、仲、叔、季碳原子,数目分别用N1、N2、N3、N4表示。例如:
中的碳原子分别称为伯、仲、叔、季碳原子,数目分别用N1、N2、N3、N4表示。例如:
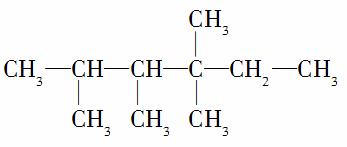
分子中,N1=6,N2=1,N3=2,N4=1。试根据不同烷烃的组成结构,分析出烷烃(除甲烷外)中各原子数的关系。
(1)烷烃分子中氢原子数N0与N1、N2、N3、N4之间的关系是N0=________________________________________________________。
(2)4种碳原子数之间的关系为N1=_______________________。
(3)若分子中N2=N3=N4=1,则该分子的结构简式可能为(任写一种)________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是( )
A.乙醇分子可以看作是乙烷分子中的一个氢原子被—OH取代而形成的
B.乙醇分子中的氢原子都可以被钠置换
C.—OH和OH-两种微粒中质子数、电子数都相等
D.水和乙醇分子中的羟基化学性质完全相同
查看答案和解析>>
科目:高中化学 来源: 题型:
电离平衡常数(用Ka表示)的大小可以判断电解质的相对强弱。25℃时,有关物质的电离平衡常数如下表所示:
| 化学式 | HF | H2CO3 | HClO |
| 电离平衡常数 (Ka) | 7.2×10-4 | K1=4.4×10-7 K2=4.7×10-11 | 3.0×10-8 |
(1)物质的量浓度均为0.1mol/L的下列四种溶液: ① Na2CO3溶液 ② NaHCO3溶液
③ NaF溶液 ④ NaClO溶液。依据数据判断pH由大到小的顺序是 。
(2)将浓度为0.1 mol/L HF溶液加水稀释一倍(假设温度不变),下列各量增大的是____。
A.c(H+) B.c(H+)·c(OH-) C.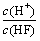 D.
D.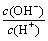
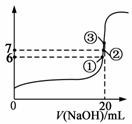 (3)25℃时,在20mL 0.1mol/L的氢氟酸溶液中加入VmL 0.1mol/L NaOH溶液,测得混合溶液的pH变化曲线如图所示,下列说法正确的是 。
(3)25℃时,在20mL 0.1mol/L的氢氟酸溶液中加入VmL 0.1mol/L NaOH溶液,测得混合溶液的pH变化曲线如图所示,下列说法正确的是 。
A.pH=3的HF溶液和pH=11的NaF溶液中,
由水电离出的c(H+)相等
B.在①点时pH=6,此时溶液中,
c(F-)-c(Na+) = 9.9×10-7mol/L
C.在②点时,溶液中的c(F-) = c(Na+)
D.在③点时V=20mL,此时溶液中c(F—) < c(Na+)=0.1mol/L
(4)在25℃时,Ksp[Cu(OH)2] =2.0×10-20。 某CuCl2溶液里C(Cu2+)= 0.02 mol·L-1,
如果要生成Cu(OH) 2沉淀,应调整溶液的pH使之大于 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com