
| A. | 丙烷没有同分异构体 | |
| B. | CH(CH3)2CH2CH2CH3的一氯代物有4种 | |
| C. | 二氯苯有3种,则四氯苯有6种 | |
| D. | CH3OH与CH2OH-CH2OH都属于醇,互为同系物 |
分析 A、丙烷只有一种结构为CH3CH2CH3;
B、根据分子中等效H原子判断,分子中由几种H原子,其一氯代物就有几种异构体;
C、若将二氯苯的氢原子换成四氯苯的氯原子,将二氯苯的氯原子换成四氯苯的氢原子,这在算同分异构体时是等效的,即二氯苯有多少同分异构体,那么四氯苯就有多少同分异构体;
D、同系物指结构相似、通式相同,组成上相差1个或者若干个CH2原子团,具有相同种类、数目的官能团的化合物.
解答 解:A、丙烷只有一种结构为CH3CH2CH3,不存在同分异构体,故A选;
B、CH(CH3)2CH2CH2CH3中有5种H原子,其一氯代物有5种,故B不选;
C、二氯苯的同分异构体有3种,二氯苯有多少同分异构体,四氯苯就有多少同分异构体,则四氯苯同分异构体的数目3种,故C不选;
D、CH3OH与CH2OH-CH2OH中含有羟基的数目不同,不是同系物,故C不选;
故选A.
点评 本题考查同分异构体、同系物的判断,难度不大,掌握判断的方法即可解答.


科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | x=0.4a,2Fe2++Cl2=2Fe3++2Cl- | |
| B. | x=1.5a,2Fe2++4Br-+3Cl2=2Br2+2Fe3++6Cl- | |
| C. | x=a,2Fe2++2Br-+2Cl2=Br2+2Fe3++4Cl- | |
| D. | x=0.6a,2Br-+Cl2=Br2+2Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Li、Na、K | B. | Na、Mg、Al | C. | Li、Be、Mg | D. | Li、Na、Mg |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 足量的溴的四氯化碳溶液 | B. | 与足量的液溴反应 | ||
| C. | 点燃 | D. | 在一定条件下与氢气加成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ③①②④ | C. | ④②③① | D. | ①③②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
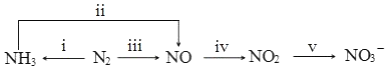
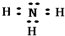 .
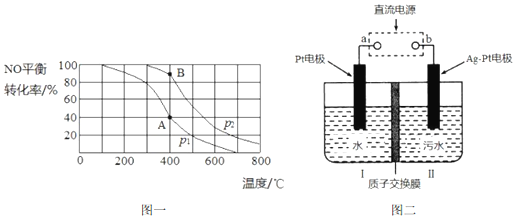
.
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
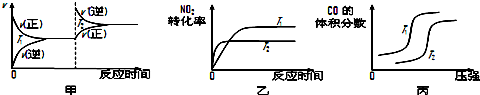
| 起始物质的量 | 甲 | 乙 | 丙 |
| n(H2O)/mol | 0.10 | 0.20 | 0.20 |
| n(CO)/mol | 0.10 | 0.10 | 0.20 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 当它们的压强和体积、温度均相同时,三种气体的质量:m(H2)>m(O2)>m(CO2) | |
| B. | 当它们的温度和压强均相同时,三种气体的密度:ρ(H2)>ρ(02)>ρ(C02) | |
| C. | 当它们的质量和温度、压强均相同时,三种气体的体积:V(CO2)>V(O2)>V(H2) | |
| D. | 当它们的温度和密度都相同时,三种气体的压强:P(H2)>P(O2)>P(CO2) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com