
【题目】氯水中含有多种成分,因而具有多种性质,根据氯水分别与如图四种物质发生的反应填空(a、b、c、d重合部分代表物质间反应,且氯水足量)。

(1)c中证明氯水含有________粒子(用粒子符号表示)。
(2)d过程中的现象是____________________,
(3)b过程中反应的离子方程式___________________。
(4)a过程中反应的化学方程式为______________。
【答案】Cl- 先变红后褪色 2H++CO32-=H2O+CO2↑ 2FeCl2+Cl2=2FeCl3
【解析】
(1)将氯气溶于水得到氯水(浅黄绿色),氯水含多种微粒,其中有H2O、Cl2、HClO、Cl-、H+、ClO-、OH-(极少量),根据离子反应证明所含粒子;
(2)氯水显酸性,且溶液中的次氯酸具有强氧化性;
(3)氯水中的盐酸与碳酸钠发生反应;
(4)氯化亚铁具有还原性,可与氯水中的氯气发生氧化还原反应。
(1)氯水中有Cl-,加入AgNO3溶液有白色沉淀生成,故c中加入硝酸银生成白色沉淀,是为了证明氯水中含有氯离子,其离子符号为:Cl-;
(2)氯水中含HCl和HClO,两者均具有酸性,可使石蕊试液变红,但HClO有强氧化性,一般在应用其漂白时,HClO的强氧化性将有色物质氧化成无色物质,所以氯水能使石蕊试液先变红后褪色,故答案为:先变红后褪色;
(3)氯水中含有HCl和HClO,具有酸性,其中HCl的酸性强于碳酸,可与碳酸钠反应生成氯化钠、二氧化碳气体和水,反应的离子方程式为CO32-+2H+=CO2↑+H2O;
(4)Cl2是新制氯水的主要成分,具有强氧化性,与FeCl2发生氧化还原反应,反应的化学方程式为2FeCl2+Cl2=2FeCl3。


 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案 导学教程高中新课标系列答案
导学教程高中新课标系列答案科目:高中化学 来源: 题型:
【题目】某温度下,体积一定的密闭容器中进行如下反应:2X(g)+Y(g)![]() Z(g)+W(s) △H>0,下列叙述正确的是
Z(g)+W(s) △H>0,下列叙述正确的是
A. 在容器中加入氩气,反应速率不变
B. 加入少量W,逆反应速率增大
C. 升高温度,正反应速率增大,逆反应速率减小
D. 将容器的体积压缩,可增大活化分子的百分数.有效碰撞次数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室欲进行0.1mol/L NaOH溶液与0.1mol/LHCl溶液的反应:
(1)写出NaOH溶液与HCl溶液反应的离子方程式___。
(2)要配制0.1mol/LNaOH溶液500mL,回答下列问题:
①需要称量NaOH固体___g;
②将NaOH固体用蒸馏水溶解后,未冷却直接转移至容量瓶,将导致所配制溶液浓度___。(填“偏大”、“偏小”或“无影响”)
③定容时,加蒸馏水至离刻度线下方1-2cm时,改用___继续滴加蒸馏水,使得溶液凹液面与刻度线相切。
(3)如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:

①该浓盐酸的物质的量浓度为___mol/L。
②欲用上述浓盐酸和蒸馏水配制0.1mol/L HCl溶液500mL,需用量筒量取___mL上述浓盐酸进行配制。
③实验室用稀盐酸溶解碳酸钙时,请写出对应的离子方程式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学教师为 “氯气与金属钠反应”设计了如图装置的实验。实验操作:先给钠预热,到钠熔融成圆球时,撤火,通入氯气,即可见钠着火燃烧,生成大量白烟。以下叙述中错误的是( )

A. 反应生成的大量白烟是氯化钠晶体
B. 玻璃管尾部塞一团浸有NaOH溶液的棉球是用于吸收过量的氯气,以免其污染空气
C. 钠着火燃烧产生苍白色火焰
D. 发生的反应为2Na+Cl2![]() 2NaCl
2NaCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)氯化铁水解的离子方程式为_________________________________,加热氯化铁溶液,蒸干并灼烧得到_______(填化学式)。
(2)25℃时,NH4Cl溶液显_________性,原因是(用离子方程式表示)__________,若加入少量的氨水,使溶液中c(NH4+)=c(Cl﹣),则溶液的pH___7(填“>”、“<”或“=”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以甲醇为燃料的新型电池,其成本大大低于以氢气为燃料的传统燃料电池,目前得到广泛的研究,如图是目前研究较多的一类固体氧化物燃料电池工作原理示意图。回答下列问题:

(1)B极上的电极反应式为 。
(2)若用该燃料电池做电源,用石墨做电极电解硫酸铜溶液,当阳极收集到11.2L(标准状况)气体时,消耗甲醇的质量为 克,若要使溶液复原,可向电解后的溶液中加入的物质有 。
(3)目前已开发出用电解法制取ClO2的新工艺。

①上图示意用石墨做电极,在一定条件下电解饱和食盐水制取ClO2。若用上述甲醇燃料电池进行电解,则电解池的电极a接甲醇燃料电池的 极( 填A或B) ,写出阳极产生ClO2的电极反应式:__________。
②电解一段时间,当阴极产生的气体体积为112 mL(标准状况)时,停止电解。通过阳离子交换膜的阳离子的物质的量为_________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组同学设计如图装置:

回答下列问题:
(1)乙中铜片为________极 (填“正”或“负”),其电极反应式为__________________
(2)若丙池盛放足量的CuSO4溶液:①在丙池铁棒这极的现象是____________________。②在丙池中阳极的电极反应是_______________________________________。
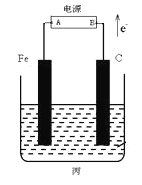
(3)若丙池中盛放滴加少量酚酞的饱和NaCl溶液1L(假设溶液体积电解前后无变化)。
①丙池通电一段时间后,___极附近溶液呈红色(填Fe或C),总反应的离子方程式:________。
②标准状况下,当丙池中有0.1mol电子发生转移时切断电源,则理论上有____ L氯气生成。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用间接电化学法可对大气污染物NO进行无害化处理,其工作原理如图所示。下列说法正确的是

A. 电极I为阴极,电极反应式为2H2O+2e一=2OH-+H2↑
B. 电解时H+由电极I向电极II迁移
C. 吸收塔中的反应为2NO+2S2O42-+2H2O=N2+4HSO3-
D. 每处理1molNO,可同时得到32gO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据元素周期表和元素周期律,判断下列叙述不正确的是

A. 气态氢化物的稳定性:H2O>NH3>SiH4
B. 氢元素与其他元素可形成共价化合物或离子化合物
C. 上图所示实验可证明元素的非金属性:Cl>C>Si
D. 用中文“![]() ”(ào)命名的第118号元素在周期表中位于第七周期0族
”(ào)命名的第118号元素在周期表中位于第七周期0族
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com